Il ferro puro (Fe) ha un punto di fusione normale di 1538 °C (1811 K / 2800 °F) a un'atmosfera; questa è la temperatura in cui la δ-ferrite (ferro cubico a corpo centrato ad alta temperatura) diventa liquida. Questo valore è il riferimento accettato nei manuali di metallurgia e nei database termochimici.
Cosa significa il punto di fusione di un metallo
Quando i metallurgisti parlano di "punto di fusione" di un metallo puro, normalmente intendono il punto di fusione di un metallo puro. temperatura di equilibrio a cui coesistono il solido cristallino e il liquido a 1 atmosfera - strettamente il normale punto di fusione (o il normale punto di congelamento). Per le leghe ingegneristiche, compresi gli acciai e le ghise, di solito c'è un punto di fusione normale (o punto di congelamento normale). intervallo di fusione tra un solidus (il primo liquido appare al riscaldamento) e un liquido (l'ultimo solido si dissolve in un liquido). Trattare i numeri di fusione numerici per i metalli come valori di riferimento che si applicano a condizioni di equilibrio molto pure; i materiali del mondo reale si comportano tipicamente in modo diverso.
Ferro puro: valori numerici e serie di dati autorevoli
Il punto di fusione normale del ferro elementare comunemente accettato è 1538 °C (1811 K / 2800 °F) alla pressione atmosferica standard. Questo valore è riportato da fonti di dati nazionali e internazionali utilizzate da ingegneri e scienziati (NIST, CRC, ASM, PDG/LBL, i principali manuali di chimica). Il normale punto di ebollizione del ferro a 1 atm è circa 2860-2862 °C (≈3134 K); i diversi riferimenti si arrotondano in modo leggermente diverso a seconda del metodo di misurazione e di valutazione.
Fatti numerici portanti:
-
Punto di fusione normale (Fe puro): 1538 °C (1811 K / 2800 °F).
-
Tipica diffusione della letteratura: ≈1535-1539 °C a seconda del metodo sperimentale e della purezza.
-
Calore latente (fusione) vicino al punto di fusione: ≈247 kJ/kg (media consigliata).
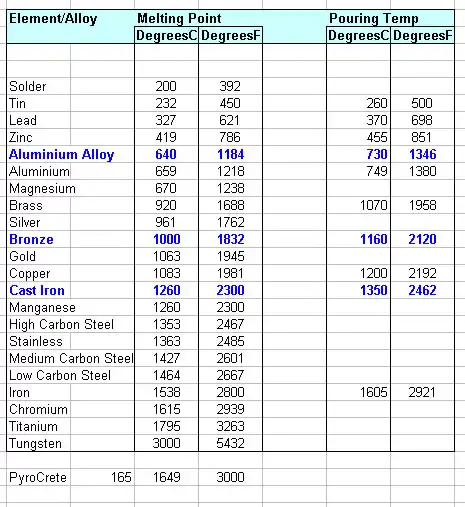
Allotropi del ferro e transizioni di fase che conducono alla fusione
Il ferro presenta forme cristalline multiple (allotropi) con la temperatura:
| Allotropo | Simbolo | Struttura cristallina | Intervallo di temperatura stabile (circa, 1 atm) |
|---|---|---|---|
| Ferro alfa | α-Fe | BCC (ferrite) | fino a 912 °C |
| Ferro gamma | γ-Fe | FCC (austenite) | 912 °C → 1394 °C |
| Ferro delta | δ-Fe | BCC (ferrite ad alta T) | 1394 °C → 1538 °C (fusione) |
| Liquido | L | - | > 1538 °C (per il Fe puro) |
Le transizioni solido → solido (α↔γ intorno a 912 °C e γ↔δ intorno a 1394 °C) sono critiche perché la fase δ è quella che fonde ai 1538 °C di riferimento. Queste temperature di transizione sono ben documentate nei diagrammi di fase e nei manuali.
Perché il numero singolo (1538 °C) è utile - e quando non lo è
Questo singolo numero è estremamente utile per il confronto e per i calcoli di base (termodinamica, set-point dei forni e storicamente nella didattica). Tuttavia, l'uso acritico di 1538 °C può trarre in inganno:
-
Leghe: L'aggiunta di carbonio, silicio, nichel, cromo o altri elementi sposta ampiamente il solidus/liquidus.
-
Impurità: Le fasi di zolfo, fosforo, ossigeno e scorie producono punti eutettici inferiori alla temperatura di fusione del Fe puro.
-
Riscaldamento non di equilibrio: Il riscaldamento rapido, il surriscaldamento o il sottoraffreddamento causano un comportamento transitorio che si discosta dall'equilibrio di fusione.
-
Pressione: L'alta pressione sposta la temperatura di fusione (rilevante per la geofisica e gli esperimenti ad alta pressione).
Pertanto, i tecnici che lavorano con acciaio, ghisa o leghe speciali dovrebbero consultare i diagrammi di fase e i dati del produttore per i valori di solidus/liquidus piuttosto che il singolo numero di Fe puro.
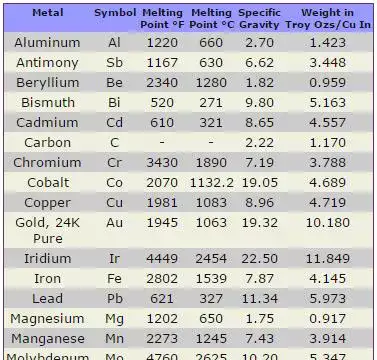
Come il carbonio influenza la temperatura di fusione del ferro
Il carbonio abbassa il punto di fusione del ferro quando forma soluzioni o carburi. Il sistema ferro-carbonio (Fe-C) è alla base della metallurgia dell'acciaio; seguono alcuni intervalli pratici:
| Materiale | Carbonio tipico (wt%) | Comportamento tipico solidus/liquidus/fusionale (circa) |
|---|---|---|
| Ferro puro | 0.00 | 1538 °C (valore singolo) |
| Acciaio a basso tenore di carbonio | 0.05-0.25 | Solidus ≈ 1450-1500 °C, Liquidus ≈ 1500-1540 °C (varia) |
| Acciaio a medio tenore di carbonio | 0.25-0.60 | Solidus ≈ 1420-1490 °C, Liquidus ≈ 1480-1530 °C |
| Acciaio ad alto tenore di carbonio / acciai per utensili | 0.6-2.0 | Il solidus può scendere ulteriormente; caratteristiche eutettiche se sono presenti altre leghe |
| Ghisa (bianco/grigio) | 2.0-4.0 | Fusione complessa con eutettici; liquidus spesso 1150-1250 °C (grafite, carburo dipendente) |
Nota: i valori di liquido/solido della ghisa variano fortemente a seconda della composizione e della pratica di fonderia - molte ghise fondono a temperature di forno sostanzialmente inferiori rispetto alla ghisa pura a causa di eutettiche e formazione di grafite. I diagrammi di fase dei frattari e del Fe-C forniscono confini dettagliati.
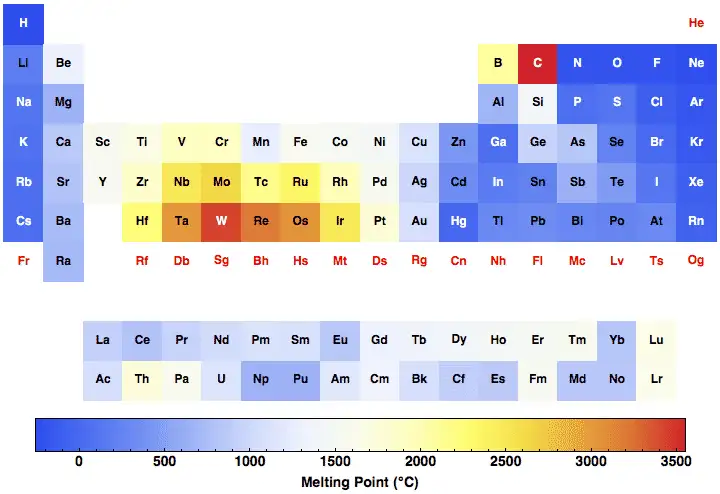
Confronto rapido: punti di fusione dei metalli comuni (tabella di riferimento)
| Elemento / materiale | Punto di fusione (°C) | Punto di fusione (°F) |
|---|---|---|
| Ferro (Fe, puro) | 1538 | 2800 |
| Rame (Cu) | 1084 | 1983 |
| Alluminio (Al) | 660.3 | 1220 |
| Nichel (Ni) | 1455 | 2651 |
| Cromo (Cr) | 1907 | 3465 |
| Titanio (Ti) | 1668 | 3034 |
| (Dati tratti da manuali standard utilizzati in ingegneria). |
Metodi di misurazione e considerazioni pratiche
La misurazione della temperatura di fusione di un metallo richiede una tecnica accurata. I metodi più comuni includono:
-
Calorimetria differenziale a scansione (DSC) / Analisi termica differenziale (DTA): Misura il flusso di calore e rileva i picchi di fusione endotermici; eccellente per campioni e leghe di piccole dimensioni.
-
Pirometria ottica ad alta temperatura con metodo a crogiolo: Per i metalli refrattari, la fusione può essere rilevata visivamente o mediante pirometria corretta per l'emissività.
-
Levitazione elettrostatica + riscaldamento laser: Utilizzato in ricerche specialistiche per evitare la contaminazione e le reazioni del crogiolo; utile per studi su liquidi surriscaldati e congelamento sottoraffreddato.
-
Metodi statici/analitici: Tecniche a goccia o a immersione storicamente utilizzate nei laboratori di metallurgia.
Ogni metodo ha fonti di incertezza: purezza del campione, interazioni crogiolo-campione, atmosfera (l'ossigeno può ossidare e modificare il comportamento apparente di fusione), velocità di riscaldamento e calibrazione. Per dati rigorosi, consultare i laboratori standard primari (NIST, istituti nazionali di metrologia).
Proprietà termofisiche intorno alla fusione
Importanti proprietà termofisiche in prossimità del punto di fusione (valori approssimativi per il Fe puro):
-
Calore latente di fusione: ≈ 247 kJ/kg (energia necessaria per fondere 1 kg al punto di fusione).
-
Variazione di densità: I metalli in genere diminuiscono la densità al momento della fusione; per il ferro la variazione dipende dal materiale e dalla fase.
-
Capacità termica: Il Cp aumenta con la temperatura; per le stime dell'energia del forno è necessario un Cp preciso rispetto alla T (il NIST e i manuali forniscono coefficienti Shomate o polinomiali adattati).
Gli ingegneri utilizzano queste proprietà per dimensionare i forni, calcolare il consumo energetico per la fusione e modellare la solidificazione nelle simulazioni di colata.
Implicazioni industriali - fusione, colata, saldatura e trattamento termico
Gli impatti pratici del comportamento di fusione del ferro includono:
-
Pratica di fonderia: Le fonderie impostano le temperature dei forni e delle siviere in modo che superino il valore di liquidità per la lega specifica; per molti acciai questo significa mantenere ~1550-1600 °C in un forno elettrico ad arco o a induzione per un corretto surriscaldamento e trasferimento della siviera. In molti casi, la ghisa fonde a temperature inferiori.
-
Saldatura: La fusione locale in saldatura richiede un controllo per evitare una diluizione eccessiva, il burn-through o l'infragilimento da parte degli elementi di lega.
-
Trattamento termico: Anche se i trattamenti termici raramente si avvicinano alla fusione, le temperature critiche di trasformazione (ad esempio, A1, A3) che determinano la microstruttura si verificano molto al di sotto della fusione, quindi si utilizzano diagrammi di fase precisi e dati TTT/CCT.
-
Fabbricazione additiva (metal AM): I tassi di fusione e solidificazione hanno un'importanza fondamentale per la microstruttura - i parametri di stampa sono regolati in base alle caratteristiche di fusione.
Buona pratica: lavorare sempre a partire dalla materiale documentato solidus/liquidus e le temperature di forno consigliate dalla fonderia o dalla cartiera, non solo il numero di fusione del Fe puro.
Pressione e condizioni estreme
A pressione ambiente il riferimento di 1538 °C è valido. Ad alta pressione, il comportamento di fusione cambia (importante per la geofisica e la ricerca sui materiali ad alta pressione). I diagrammi di fase sperimentali e calcolati a pressioni di GPa mostrano che la temperatura di fusione può aumentare con la pressione per il Fe; tali spostamenti sono al di fuori della normale rilevanza industriale, ma sono fondamentali per la modellazione del nucleo terrestre e per i dispositivi ad alta pressione. Pubblicazioni specializzate e riassunti del NIST/PDG documentano le linee di fusione dipendenti dalla pressione.
Errori comuni e come evitarli
-
Utilizzo del numero di Fe puro per le leghe: porta a impostazioni errate del forno. Utilizzare sempre i dati specifici del materiale.
-
Confondere il punto di fusione con il solidus/liquidus: per le leghe si tratta di intervalli, non di valori singoli.
-
Ignorare l'atmosfera e la contaminazione: Le reazioni di ossidazione o di crogiolo alterano il comportamento di fusione. Se necessario, utilizzare gas inerti o il vuoto.
-
Affidarsi a termocoppie o pirometri non calibrati: La calibrazione riconducibile a standard è essenziale per ottenere temperature precise.
Tavole pratiche per ingegneri
Intervalli solidus/liquidus rappresentativi (ingegneria circa)
| Famiglia di materiali | Esempio di composizione | Solidus circa (°C) | Liquido approssimativo (°C) | Note |
|---|---|---|---|---|
| Ferro puro | 0% C | 1538 (singolo) | 1538 | Riferimento Fe puro |
| Acciaio a basso tenore di carbonio | 0,05-0,25% C | 1450-1500 | 1500-1540 | Dipende dalla lega |
| Acciaio inossidabile (austenitico) | Fe-18Cr-8Ni | ~1390-1450 | ~1450-1520 | Ni/Cr innalzano o abbassano il comportamento locale di fusione |
| Ghisa grigia | 2-4% C (grafite) | ~1150 | ~1200-1250 | Caratteristiche eutettiche con la grafite |
Domande frequenti
-
Q: Qual è il punto di fusione del ferro?
A: 1538 °C (1811 K / 2800 °F) per il ferro elementare a 1 atm. -
Q: L'acciaio fonde alla stessa temperatura del ferro puro?
A: No. L'acciaio è una lega e presenta una fusione gamma (da solido a liquido) che dipende dal carbonio e dal contenuto di lega; molti acciai fondono al di sotto o vicino al numero di Fe puro. -
Q: Perché le fonderie utilizzano temperature di forno superiori a 1538 °C?
A: Manutenzione dei forni surriscaldamento al di sopra del liquido per garantire una buona fluidità, il tempo per il degassamento e per compensare le perdite di calore durante il trasferimento. I riscaldamenti tipici dell'acciaio sono spesso mantenuti a ~1550-1600 °C, a seconda della lega e del processo. -
Q: In che modo la concentrazione di carbonio influenza la fusione?
A: Il carbonio abbassa i punti di fusione attraverso reazioni eutettiche; le ghise (ad alto contenuto di C) hanno in genere temperature di fusione molto più basse del ferro puro. Vedi diagrammi di fase Fe-C. -
Q: Le impurità possono aumentare il punto di fusione?
A: Alcuni elementi aumentano e altri abbassano il liquidus; ad esempio, il cromo e il tungsteno aumentano tipicamente la resistenza alle alte temperature e possono aumentare il comportamento di fusione in alcune leghe, mentre il carbonio e lo zolfo abbassano alcuni limiti di fusione. Gli effetti esatti dipendono dalla composizione. -
Q: Quanto sono precisi i 1538 °C?
A: Le diverse fonti autorevoli si discostano leggermente; i valori sperimentali possono variare di qualche °C a seconda della purezza e del metodo di misurazione. La diffusione tipica riportata è di ~1535-1539 °C. -
Q: Qual è il calore latente di fusione del ferro?
A: Approssimativamente 247 kJ/kg, utilizzato per il budget energetico per la fusione. -
Q: L'ossigeno atmosferico modifica il comportamento effettivo della fusione?
A: Sì, l'ossidazione, la formazione di strati di scorie e ossidi e le reazioni del crogiolo possono modificare il comportamento apparente della fusione e devono essere controllate con flussi, gestione delle scorie o atmosfere inerti. -
Q: Esistono riferimenti standard per i punti di fusione?
A: Sì! Il NIST WebBook, il CRC Handbook, i manuali ASM e le tabelle PDG/LBL sono ampiamente utilizzati per ottenere dati termofisici affidabili. -
Q: Dove posso trovare il solidus/liquidus per una specifica qualità di acciaio industriale?
A: Consultare la scheda tecnica del produttore dell'acciaio, i riferimenti standard (ad esempio, ASM, diagrammi di fase Fe-C e multicomponente pubblicati) o i database termodinamici (ad esempio, Thermo-Calc, FactSage) per ottenere dati accurati sui confini di fase.
Note finali per i professionisti
-
Utilizzare il 1538 °C solo come base di riferimento per il ferro puro.
-
Per il controllo del processo, fare sempre affidamento su solidus/liquidus specifici del materiale, sulle schede tecniche della cartiera/fonderia e sulla strumentazione calibrata.
-
Per le pubblicazioni o i lavori di progettazione, citare le banche dati autorevoli (NIST/CRC/ASM) e indicare le condizioni (pressione, atmosfera, composizione) in cui si applicano le temperature.
Riferimenti autorevoli
- NIST Chemistry WebBook - Dati termochimici e di fase condensata del ferro (Fe)
- PubChem / NCBI - Riassunto e dati fisici del ferro (elemento) (include riferimenti CRC)
- Particle Data Group / LBL - Dati atomici e di fase del Fe (ferro) (temperature di fusione/ebollizione)
- ASM International - Manuali sui metalli e capitoli sulle proprietà dei metalli puri (richiede accesso)
- Risorse per il diagramma di fase Fe-C e materiale esplicativo (riassunti accademici/libri)

