I metalli sono elementi che tipicamente conducono elettricità e calore, mostrano una lucentezza metallica, si deformano plasticamente sotto sforzo e cedono elettroni nelle reazioni chimiche; i non metalli di solito non hanno lucentezza metallica, sono scarsi conduttori elettrici, tendono a guadagnare o condividere elettroni e formano ossidi covalenti o acidi; i metalloidi mostrano un comportamento ibrido, possedendo una miscela di proprietà metalliche e non metalliche che li rendono preziosi nei semiconduttori e nelle leghe specializzate.
Classificazione storica e motivazioni
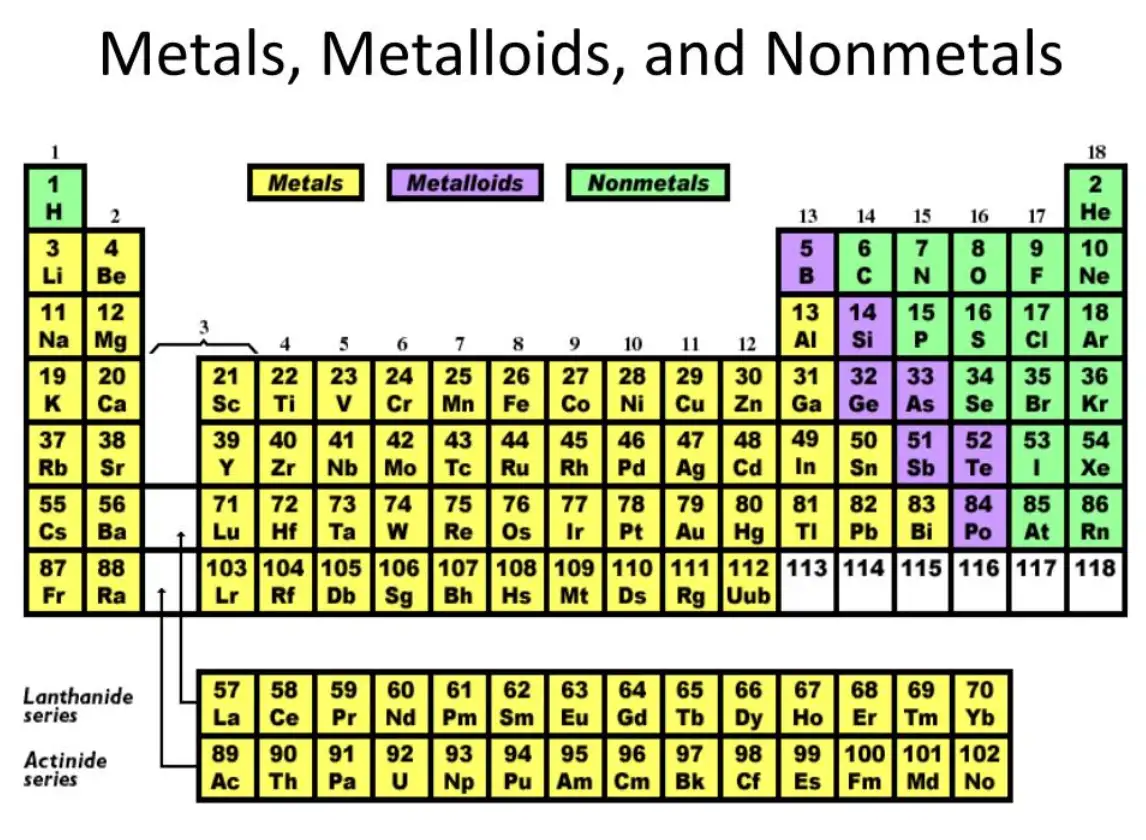
La classificazione degli elementi in metalli e non metalli risale ai primi tempi della chimica e della mineralogia, quando proprietà come la malleabilità, la lucentezza e la capacità di formare leghe erano caratteristiche primarie di selezione. Lo sviluppo della tavola periodica ha perfezionato il sistema: i gruppi a sinistra e al centro sono prevalentemente metallici, i gruppi a destra sono in gran parte non metallici, con una stretta fascia diagonale di elementi che presentano caratteristiche miste: i metalloidi. I fattori pratici che hanno spinto alla classificazione sono stati: l'utilità metallurgica, la facilità di estrazione, l'importanza economica e la previsione del comportamento chimico. Nella pratica moderna, la classificazione supporta la selezione dei materiali, la progettazione dei processi e la modellazione predittiva.
Definizione delle proprietà: criteri fisici
Una lista di controllo tecnica utile durante l'identificazione:
-
Conducibilità elettrica: Elevata nella maggior parte dei metalli a causa di un mare di elettroni delocalizzati. Bassa nella maggior parte dei non metalli. I metalloidi spesso presentano una conduttività semiconduttiva che cambia fortemente con la temperatura e il drogaggio.
-
Conduttività termica: I metalli in genere conducono il calore in modo efficiente; i non metalli hanno una conduzione termica più scarsa; i metalloidi variano.
-
Lucentezza e riflettività: I metalli mostrano una caratteristica lucentezza metallica e un'elevata riflettività sulle superfici lucidate; molti non metalli sono opachi o trasparenti; i metalloidi spesso mostrano una tenue lucentezza metallica.
-
Malleabilità e duttilità: I metalli si deformano plasticamente sotto sforzo permettendo la laminazione, la forgiatura o la trafilatura; i non metalli sono fragili in forma solida in massa; i metalloidi possono essere fragili ma talvolta possono essere lavorati in condizioni particolari.
-
Resistenza meccanica: I metalli spaziano da quelli teneri (ad esempio, il sodio) a quelli estremamente resistenti (ad esempio, gli acciai ad alta resistenza); le prestazioni meccaniche dipendono fortemente dalla microstruttura e dalle leghe.
-
Densità: I metalli hanno in genere densità più elevate dei non metalli, anche se esistono eccezioni (ad esempio, lo iodio, non metallo denso).
-
Fase a STP (temperatura e pressione standard): La maggior parte dei metalli è solida a STP (il mercurio è un'importante eccezione liquida). I non metalli possono essere gas (O₂, N₂), liquidi (bromo) o solidi (carbonio, zolfo).
Definizione delle proprietà: comportamento chimico e tendenze al legame
Le differenze chimiche derivano dall'elettronegatività, dall'energia di ionizzazione e dall'affinità elettronica:
-
Tendenza a perdere elettroni: I metalli hanno energie di ionizzazione relativamente basse e formano facilmente cationi. Formano legami ionici con molti non metalli e legami metallici in forma pura o in lega.
-
Tendenza a guadagnare o condividere elettroni: I non metalli hanno elettronegatività ed energie di ionizzazione più elevate, che favoriscono il guadagno o la condivisione di elettroni; formano reti covalenti, molecole biatomiche o anioni poliatomici.
-
Carattere di ossido: Gli ossidi metallici tendono a essere basici o anfoteri, mentre gli ossidi non metallici sono spesso acidi; i metalloidi possono formare ossidi anfoteri che mostrano entrambi i comportamenti a seconda del partner di reazione.
-
Comportamento redox in ambienti tipici: I metalli agiscono come agenti riducenti a contatto con ambienti acidi; i non metalli spesso ossidano i metalli o agiscono come ossidanti, se necessario.
-
Formazione complessa: I metalli di transizione formano facilmente complessi di coordinazione grazie alla partecipazione degli orbitali d; i non metalli e i metalloidi partecipano in modo diverso alla chimica dei complessi.
Struttura elettronica e disposizione periodica
La comprensione della posizione di ciascuna categoria nella tavola periodica chiarisce sia le tendenze che le eccezioni:
-
Metalli: Occupano il blocco s, il blocco d, il blocco f e parte del blocco p. Sono caratterizzati da bande di conduzione parzialmente riempite e da funzioni di lavoro basse. I metalli di transizione (blocco d) mostrano stati di ossidazione variabili e proprietà magnetiche e catalitiche complesse.
-
Non metalli: Si raggruppano verso l'alto a destra della tavola periodica (esclusi i gas nobili che sono una categoria a parte). I piccoli raggi atomici, le elevate elettronegatività e i gusci di valenza pieni o quasi pieni producono un forte legame direzionale.
-
Metalloidi: A cavallo tra metalli e non metalli: boro, silicio, germanio, arsenico, antimonio, tellurio, polonio (le classificazioni variano). Le loro strutture a banda creano strette lacune di banda adatte alle applicazioni dei semiconduttori.
Metalloidi: definizione, identificazione e comportamento borderline
I metalloidi meritano un'attenzione particolare perché le loro proprietà intermedie sono alla base dell'elettronica moderna e delle leghe speciali:
-
Metalloidi canonici: Boro (B), Silicio (Si), Germanio (Ge), Arsenico (As), Antimonio (Sb), Tellurio (Te). Il polonio è talvolta incluso, ma ha considerazioni radioattive.
-
Perché i metalloidi sono importanti: Il loro comportamento semiconduttivo può essere regolato mediante drogaggio e temperatura; formano fasi vetrose e ceramiche con i non metalli; funzionano come elementi di lega che modificano le proprietà meccaniche e termiche.
-
Forme strutturali: Molti metalloidi formano reti covalenti (ad esempio, il silicio) che sono fragili ma elettricamente attive quando vengono drogate. Altri (ad esempio, l'antimonio) hanno strutture cristalline stratificate che mostrano un comportamento anisotropo.
-
Ruolo industriale: Semiconduttori (Si, Ge), ritardanti di fiamma e modificatori di leghe (Sb), materiali termoelettrici (Te) e ceramiche speciali (B).
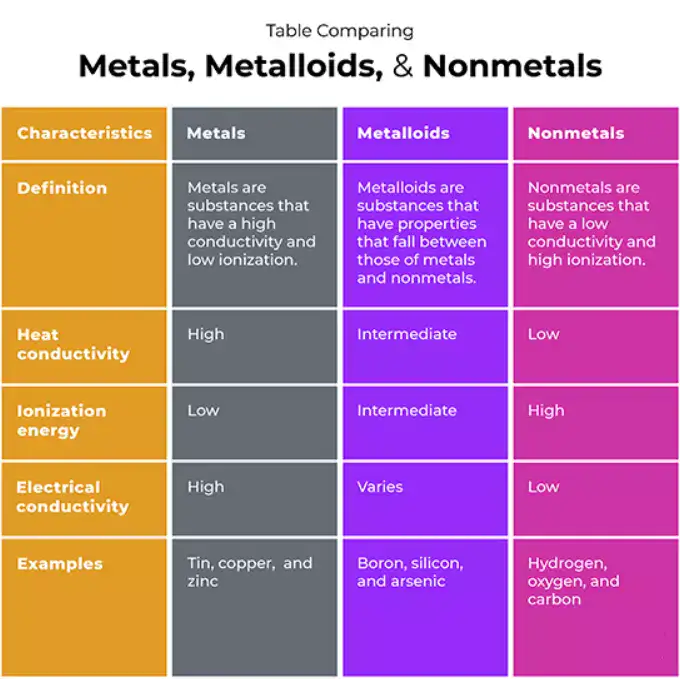
Tabelle comparative - riferimento rapido
Tabella 1 - Confronto fisico e chimico di alto livello
| Proprietà / Caratteristica | Metalli | Non metalli | Metalloidi |
|---|---|---|---|
| Conducibilità elettrica tipica | Alto | Basso o nullo | Intermedio / semiconduttore |
| Conducibilità termica | Alto | Basso | Moderato |
| Lustro | Metallizzato (lucido) | Opaco / non metallico | Spesso lucentezza metallica |
| Comportamento meccanico | Duttile / malleabile (molti) | Fragile (la maggior parte dei solidi) | Da fragile a semi-duttile |
| Ossidi comuni | Base / anfotero | Acido / covalente | Anfotero |
| Incollaggio tipico | Metallico / ionico | Covalente / molecolare | Covalente con parziale carattere metallico |
| Posizione periodica | Sinistra / centro / fondo | Destra / superiore | Limite della scala |
Tabella 2 - Esempi rappresentativi e usi tipici
| Categoria | Elementi rappresentativi | Usi industriali tipici |
|---|---|---|
| Metalli | Ferro (Fe), Rame (Cu), Alluminio (Al), Nichel (Ni), Titanio (Ti) | Acciaio strutturale, cablaggio elettrico, aerospaziale, leghe resistenti alla corrosione |
| Non metalli | Ossigeno (O), Azoto (N), Zolfo (S), Carbonio (C), Fosforo (P) | Materie prime chimiche, polimeri, ossidanti, catalizzatori (supporti di carbonio) |
| Metalloidi | Silicio (Si), germanio (Ge), boro (B), antimonio (Sb), tellurio (Te) | Semiconduttori, termoelettrici, ceramiche speciali, additivi per leghe |
Tabella 3 - Firma elettronica / incollaggio e note di estrazione
| Classe dell'elemento | Comportamento degli elettroni di valenza | Fonte di minerale tipica | Tipico percorso di estrazione o lavorazione |
|---|---|---|---|
| Metalli | Elettroni di conduzione delocalizzati | Minerali: ossidi, solfuri | Pirometallurgia, idrometallurgia, raffinazione elettrolitica |
| Non metalli | Localizzazione degli elettroni, reti covalenti | Gas nativi, depositi minerali (ad esempio, di zolfo), fonti organiche | Sintesi chimica, separazione dei gas, estrazione mineraria (ad esempio, grafite) |
| Metalloidi | Banda passante stretta, legami covalenti direzionali | Silicati, solfuri, forme native | Purificazione chimica (raffinazione a zone per il Si), torrefazione e lisciviazione |

Presenza geologica, estrazione e forme commerciali
Dal punto di vista dell'approvvigionamento e della lavorazione:
-
Metalli: Spesso estratto da ossidi e minerali solforati (ad esempio, ematite per il ferro, calcopirite per il rame). La fusione rimuove l'ossigeno o lo zolfo; l'elettroraffinazione e le fasi magnetoidrometallurgiche producono metallo di elevata purezza. Forme commerciali: lingotti, billette, lamiere, bobine, fili, polveri.
-
Non metalli: Si presentano in forme elementari, molecolari o minerali. Il carbonio si presenta sotto forma di grafite o diamante; lo zolfo si trova in depositi elementari o emissioni vulcaniche; l'azoto e l'ossigeno sono gas atmosferici ottenuti per separazione dell'aria. Le forme commerciali includono gas, polveri e solidi molecolari.
-
Metalloidi: Il silicio viene estratto dal quarzo e raffinato per ottenere silicio di grado metallurgico tramite riduzione carbotermica, quindi purificato con metodi chimici (ad esempio, il processo Siemens o i reattori a letto fluido) per ottenere Si di grado elettronico. Il boro è ottenuto dai borati; il germanio è spesso recuperato da minerali di zinco o ceneri volanti di carbone.
Usi ed esempi industriali con note pratiche di approvvigionamento
Riassunti elemento per elemento con considerazioni sull'acquisto:
-
Ferro / Acciaio (metallo): Metallo strutturale primario. Le specifiche di acquisto di solito fanno riferimento a standard (ASTM A36, A992, ecc.) e alla microstruttura (ad esempio, ferritica, martensitica). La resistenza alla corrosione e la saldabilità dipendono dalla composizione e dal trattamento termico.
-
Rame (metallo): Fondamentale per la conduzione elettrica. I gradi di acquisto (ad esempio, C11000, C10200) indicano purezza e conduttività. Il rame privo di ossigeno viene utilizzato quando sono richiesti un'elevata conduttività e bassi livelli di impurità.
-
Alluminio (metallo): Da preferire nei casi in cui la bassa densità e la resistenza alla corrosione sono fondamentali. Le serie di leghe (da 1000 a 7000) definiscono le proprietà chiave. La finitura superficiale e la tempra sono importanti per le applicazioni di formatura o strutturali.
-
Silicio (metalloide): Silicio di grado elettronico usato per i wafer; silicio di grado metallurgico usato per leghe e siliconi. L'acquisto richiede un'attenzione particolare alla purezza (livelli di ppb per l'elettronica).
-
Carbonio (non metallo): Grafite utilizzata come elettrodo ad alta temperatura e lubrificante; carbone attivo per l'adsorbimento. Le forme e la porosità regolano le prestazioni.
Suggerimento per l'approvvigionamento: richiedere i certificati dei materiali (rapporti di prova della cartiera, rapporti di prova chimici e meccanici), confermare i limiti di impurità in tracce per le applicazioni critiche e verificare la conformità agli standard applicabili (ASTM, ISO, EN).
Leghe, trattamenti e modifiche delle proprietà
Come le differenze si adattano ai processi industriali comunemente utilizzati:
-
Metalli di lega: L'incorporazione di elementi modifica la densità degli elettroni, la distorsione del reticolo e la stabilità di fase. Ad esempio, il carbonio nel ferro forma un acciaio con una resistenza notevolmente maggiore; il cromo aggiunge resistenza alla corrosione negli acciai inossidabili.
-
Doping dei metalloidi: L'introduzione controllata di impurità donatrici o accettoriali converte i semiconduttori intrinseci in n-tipo o p-tipo, determinando il comportamento elettrico. La temperatura e la concentrazione regolano la mobilità dei portatori.
-
Funzionalizzazione non metallica: I non metalli formano composti funzionali (ad esempio, il carbonio nei polimeri, lo zolfo nella gomma vulcanizzata) che forniscono specifiche prestazioni chimiche o meccaniche.
-
Trattamento termico: I metalli rispondono bene a ricottura, tempra, rinvenimento e invecchiamento. I metalli e i materiali non metallici richiedono percorsi termici o chimici specializzati per la regolazione delle proprietà (ad esempio, sinterizzazione della ceramica, ricottura del vetro).
Sicurezza, manipolazione e considerazioni ambientali
Punti pratici di sicurezza per ogni classe:
-
Metalli: Molti metalli producono polveri o fumi tossici durante il taglio, la saldatura o la fusione (ad esempio, piombo, cadmio). I metalli corrosi possono produrre sottoprodotti pericolosi. Utilizzare DPI appropriati, ventilazione e rispettare le norme sullo smaltimento dei rifiuti.
-
Non metalli: I non metalli reattivi (ad es. fosforo, cloro gassoso) comportano rischi acuti; le polveri (ad es. nerofumo) possono presentare rischi di esplosione di polveri. Seguire le indicazioni della scheda di sicurezza.
-
Metalloidi: Alcuni metalloidi presentano problemi di tossicità (ad esempio, i composti dell'arsenico). I materiali semiconduttori possono richiedere il controllo della contaminazione e la manipolazione in camera bianca.
-
Ambientale: Gli impatti del ciclo di vita variano notevolmente; i metalli spesso comportano un'estrazione ad alta intensità energetica, mentre la produzione di alcuni non metalli (come i polimeri di derivazione petrolchimica) comporta diversi profili di inquinanti. Le considerazioni sul riciclo e la sostituzione giocano un ruolo importante nella strategia di approvvigionamento.
Come identificare un campione sconosciuto in laboratorio o in officina
Un protocollo pratico a tappe:
-
Ispezione visiva: Osservare il colore, la lucentezza e la consistenza. La lucentezza metallica suggerisce un metallo o un metalloide.
-
Misura della densità: La densità di massa misurata mediante spostamento fornisce un forte indizio. Un'alta densità suggerisce la presenza di metalli (ma controllate la presenza di non metalli pesanti come lo iodio).
-
Test elettrico: Utilizzare un multimetro per misurare la conduttività CC. Un'alta conduttività indica un metallo; una bassa indica un non metallo; un comportamento intermedio dipendente dalla temperatura indica un metalloide/semiconduttore.
-
Test meccanico: Semplici test di piegatura o di graffiatura indicano la duttilità rispetto alla fragilità. I metalli tipicamente si deformano; i non metalli spesso si fratturano.
-
Test chimici a campione: La reazione di piccoli campioni con acidi o l'uso di test alla fiamma possono identificare il comportamento della classe: i metalli possono dissolversi formando ioni colorati; i non metalli producono gas o residui insolubili. Seguire sempre i protocolli di sicurezza.
-
Conferma spettroscopica: XRF, AES, ICP-MS o XRD forniscono la composizione definitiva e l'identificazione delle fasi per la verifica del grado di approvvigionamento.
Domande frequenti
D1: Quale differenza elettronica fondamentale separa i metalli dai non metalli?
A: I metalli possiedono elettroni di valenza delocalizzati che formano bande di conduzione, consentendo il movimento di elettroni liberi sotto un campo elettrico. I non metalli hanno elettroni localizzati che occupano gusci di valenza pieni o quasi pieni, sostenendo legami covalenti direzionali e determinando una scarsa conduzione elettrica in massa.
D2: I metalloidi sono sempre semiconduttori?
A: Non sempre. Molti metalloidi hanno un comportamento semiconduttore intrinseco con strette lacune di banda (esempio: silicio, germanio), ma la forma fisica, il drogaggio e la temperatura influenzano fortemente la conduttività; alcuni metalloidi si comportano in modo più metallico in particolari morfologie cristalline.
D3: In che modo le proprietà degli ossidi riflettono la classificazione degli elementi?
A: Gli ossidi metallici sono tipicamente basici o anfoteri e neutralizzano gli acidi per formare sali. Gli ossidi non metallici sono solitamente acidi e formano acidi in acqua (ad esempio, SO₂ → acido solforoso). I metalloidi formano comunemente ossidi anfoteri con reazioni sia basiche che acide.
D4: Quali test determinano rapidamente se un metallo è un metallo di transizione o un metallo del gruppo principale?
A: I metalli di transizione mostrano in genere più stati di ossidazione stabili, ioni colorati in soluzione e un comportamento di formazione di complessi; i metalli del gruppo principale mostrano in genere meno stati di ossidazione e composti binari più semplici.
D5: Quanto è importante la purezza del silicio industriale utilizzato nell'elettronica?
A: Estremamente importante. Il silicio per uso elettronico richiede livelli di impurità nell'ordine delle parti per miliardo (ppb) o inferiori; le tracce di metalli possono alterare drasticamente la durata del vettore e la resa del dispositivo.
D6: I non metalli possono formare leghe?
A: Non nel senso classico del metallo. Tuttavia, gli elementi non metallici si combinano per formare miscele e compositi (ad esempio, il carbonio nei compositi rinforzati con grafite o nelle miscele di polimeri) che svolgono funzioni simili alle leghe in alcune applicazioni.
D7: Quale classe si corrode più facilmente e come si ottiene la protezione?
A: La propensione alla corrosione dipende dall'ambiente e dall'elemento: il ferro arrugginisce facilmente in presenza di ossigeno umido; molti non metalli non si corrodono ma possono ossidarsi o decomporsi. I metodi di protezione comprendono rivestimenti, protezione catodica, leghe e controllo ambientale.
D8: Ci sono elementi che sfuggono a una semplice classificazione?
A: Sì. Diversi elementi si trovano vicino al confine metalloide e mostrano un polimorfismo con fasi metalliche e non metalliche. Inoltre, gli elementi sottoposti a pressioni o temperature estreme possono cambiare comportamento.
D9: In che modo le aggiunte di leghe di metalloidi influenzano le proprietà dei metalli?
A: Piccole aggiunte di metalloidi (ad esempio, silicio, boro) affinano la dimensione dei grani, alterano la temprabilità, migliorano la resistenza alla temperatura o modificano il comportamento elettrico. Ad esempio, il silicio nell'acciaio influenza la disossidazione e le proprietà magnetiche.
Q10: Quali norme sui materiali devono essere consultate quando si specificano i metalli per l'approvvigionamento?
A: Gli standard comuni includono ASTM (americani), EN (europei), ISO, JIS (giapponesi) a seconda della regione. Per i materiali elettronici, si applicano gli standard JEDEC e quelli specifici per i semiconduttori. Richiedete sempre i rapporti di prova delle cartiere e i documenti di conformità.
Riferimenti autorevoli
- IUPAC - Tavola periodica e informazioni sugli elementi
- NIST Chemistry WebBook - Dati termochimici e spettroscopici
- Royal Society of Chemistry - Tavola periodica interattiva e dati sugli elementi
- USGS - Informazioni su metalli e minerali (Centro nazionale di informazione sui minerali)
Note conclusive e passi successivi consigliati
-
Per la documentazione relativa agli appalti, abbinare questo materiale concettuale alle norme ASTM/EN applicabili per ogni specifico metallo o lega.
-
Per chi prepara materiale didattico o contenuti web, trasformare le tabelle in HTML responsive con microdati per ottenere risultati più ricchi sui motori di ricerca.
-
Se sono necessari ulteriori dettagli su un singolo elemento, un sistema di leghe o un percorso di lavorazione (ad esempio, programmi di trattamento termico per acciai specifici, percorsi di purezza dei wafer di silicio o dati sui test di corrosione), fornire il nome dell'elemento o della lega e l'applicazione prevista; è quindi possibile preparare un brief tecnico mirato.

