Metalle sind Elemente, die in der Regel Elektrizität und Wärme leiten, metallisch glänzen, sich unter Belastung plastisch verformen und bei chemischen Reaktionen Elektronen abgeben; Nichtmetalle haben in der Regel keinen metallischen Glanz, sind schlechte elektrische Leiter, neigen dazu, Elektronen zu gewinnen oder zu teilen und bilden kovalente oder saure Oxide; Metalloide zeigen ein hybrides Verhalten, d. h. sie besitzen eine Mischung aus metallischen und nichtmetallischen Eigenschaften, die sie für Halbleiter und spezielle Legierungen wertvoll machen.
Historische Einordnung und Begründung
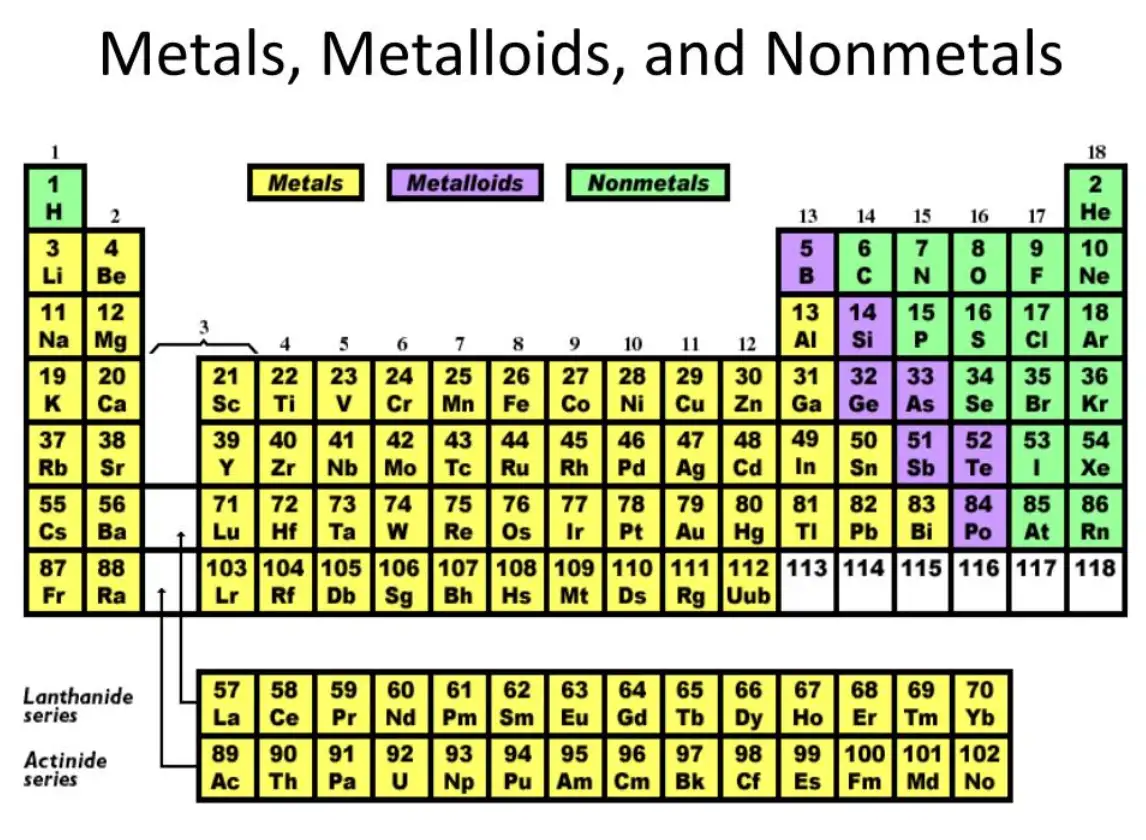
Die Einteilung der Elemente in Metalle und Nichtmetalle geht auf die frühe Chemie und Mineralogie zurück, als Eigenschaften wie Formbarkeit, Glanz und die Fähigkeit zur Bildung von Legierungen die wichtigsten Sortiermerkmale waren. Mit der Entwicklung des Periodensystems wurde das System verfeinert: Die Gruppen links und in der Mitte sind überwiegend metallisch, die Gruppen rechts davon sind größtenteils nichtmetallisch, mit einem schmalen diagonalen Band von Elementen, die gemischte Eigenschaften aufweisen: die Metalloide. Zu den praktischen Triebkräften für die Klassifizierung gehörten: metallurgischer Nutzen, leichte Gewinnbarkeit, wirtschaftliche Bedeutung und vorhersagbares chemisches Verhalten. In der modernen Praxis unterstützt die Klassifizierung die Materialauswahl, die Prozessgestaltung und die vorausschauende Modellierung.
Definierende Eigenschaften: physikalische Kriterien
Eine technische Checkliste, die bei der Identifizierung nützlich ist:
-
Elektrische Leitfähigkeit: Hoch in den meisten Metallen aufgrund eines Meeres von delokalisierten Elektronen. Niedrig in den meisten Nichtmetallen. Metalloide weisen oft eine halbleitende Leitfähigkeit auf, die sich je nach Temperatur und Dotierung stark verändert.
-
Wärmeleitfähigkeit: Metalle leiten Wärme in der Regel gut; Nichtmetalle haben eine schlechtere Wärmeleitung; Metalloide variieren.
-
Glanz und Reflexionsvermögen: Metalle weisen einen charakteristischen Metallglanz und ein hohes Reflexionsvermögen auf polierten Oberflächen auf; viele Nichtmetalle sind matt oder transparent; Metalloide zeigen oft einen gedämpften Metallglanz.
-
Verformbarkeit und Duktilität: Metalle verformen sich unter Spannung plastisch, so dass sie gewalzt, geschmiedet oder gezogen werden können; Nichtmetalle sind in fester Form spröde; Metalloide können spröde sein, lassen sich aber manchmal unter speziellen Bedingungen bearbeiten.
-
Mechanische Festigkeit: Metalle umfassen ein breites Spektrum von weich (z. B. Natrium) bis extrem fest (z. B. hochfeste Stähle); die mechanische Leistung hängt stark von der Mikrostruktur und der Legierung ab.
-
Die Dichte: Metalle haben im Allgemeinen eine höhere Dichte als Nichtmetalle, obwohl es auch Ausnahmen gibt (z. B. das dichte Nichtmetall Jod).
-
Phase bei STP (Standardtemperatur und -druck): Die meisten Metalle sind bei STP fest (Quecksilber ist eine wichtige flüssige Ausnahme). Nichtmetalle können Gase (O₂, N₂), Flüssigkeiten (Brom) oder Feststoffe (Kohlenstoff, Schwefel) sein.
Definierende Eigenschaften: chemisches Verhalten und Bindungstendenzen
Chemische Unterschiede ergeben sich aus Elektronegativität, Ionisierungsenergie und Elektronenaffinität:
-
Neigung, Elektronen zu verlieren: Metalle haben eine relativ geringe Ionisierungsenergie und bilden leicht Kationen. Sie bilden Ionenbindungen mit vielen Nichtmetallen und metallische Bindungen in reiner Form oder in Legierungen.
-
Neigung, Elektronen zu gewinnen oder zu teilen: Nichtmetalle weisen höhere Elektronegativitäten und Ionisierungsenergien auf, was den Gewinn oder die gemeinsame Nutzung von Elektronen begünstigt; sie bilden kovalente Netzwerke, zweiatomige Moleküle oder mehratomige Anionen.
-
Oxid-Charakter: Metalloxide sind in der Regel basisch oder amphoter, während Nichtmetalloxide häufig sauer sind; Metalloide können amphotere Oxide bilden, die je nach Reaktionspartner beide Verhaltensweisen zeigen.
-
Redoxverhalten in typischen Umgebungen: Metalle wirken als Reduktionsmittel in Kontakt mit sauren Umgebungen; Nichtmetalle oxidieren häufig Metalle oder wirken gegebenenfalls als Oxidationsmittel.
-
Komplexe Bildung: Übergangsmetalle bilden aufgrund der Beteiligung des d-Orbitals leicht Koordinationskomplexe; Nichtmetalle und Metalloide beteiligen sich anders an der Komplexchemie.
Elektronische Struktur und periodische Anordnung
Wenn man versteht, wo jede Kategorie im Periodensystem auftaucht, werden sowohl Trends als auch Ausnahmen deutlich:
-
Metalle: Besetzen den s-Block, d-Block, f-Block und einen Teil des p-Blocks. Sie zeichnen sich durch teilweise gefüllte Leitungsbänder und niedrige Arbeitsfunktionen aus. Übergangsmetalle (d-Block) weisen variable Oxidationsstufen und komplexe magnetische und katalytische Eigenschaften auf.
-
Nichtmetalle: Cluster rechts oben im Periodensystem (mit Ausnahme der Edelgase, die in einer eigenen Kategorie aufgeführt sind). Kleine Atomradien, hohe Elektronegativitäten und gefüllte oder fast gefüllte Valenzschalen führen zu einer starken gerichteten Bindung.
-
Metalloide: Auf der Treppe zwischen Metallen und Nichtmetallen: Bor, Silizium, Germanium, Arsen, Antimon, Tellur, Polonium (unterschiedliche Klassifizierungen). Ihre Bandstrukturen schaffen schmale Bandlücken, die für Halbleiteranwendungen geeignet sind.
Metalloide: Definition, Identifizierung und grenzwertiges Verhalten
Metalloide verdienen besondere Aufmerksamkeit, da ihre Zwischeneigenschaften die Grundlage für moderne Elektronik und Speziallegierungen bilden:
-
Kanonische Metalloide: Bor (B), Silizium (Si), Germanium (Ge), Arsen (As), Antimon (Sb), Tellur (Te). Polonium ist manchmal enthalten, hat aber radioaktive Eigenschaften.
-
Warum Metalloide wichtig sind: Ihr halbleitendes Verhalten kann durch Dotierung und Temperatur eingestellt werden; sie bilden glasartige und keramische Phasen mit Nichtmetallen; sie fungieren als Legierungselemente, die mechanische und thermische Eigenschaften verändern.
-
Strukturelle Formen: Viele Metalloide bilden kovalente Netzwerke (z. B. Silizium), die spröde, aber elektrisch aktiv sind, wenn sie dotiert sind. Andere (z. B. Antimon) haben geschichtete Kristallstrukturen, die anisotropes Verhalten zeigen.
-
Industrielle Rolle: Halbleiter (Si, Ge), Flammschutzmittel und Legierungszusätze (Sb), thermoelektrische Materialien (Te) und Spezialkeramik (B).
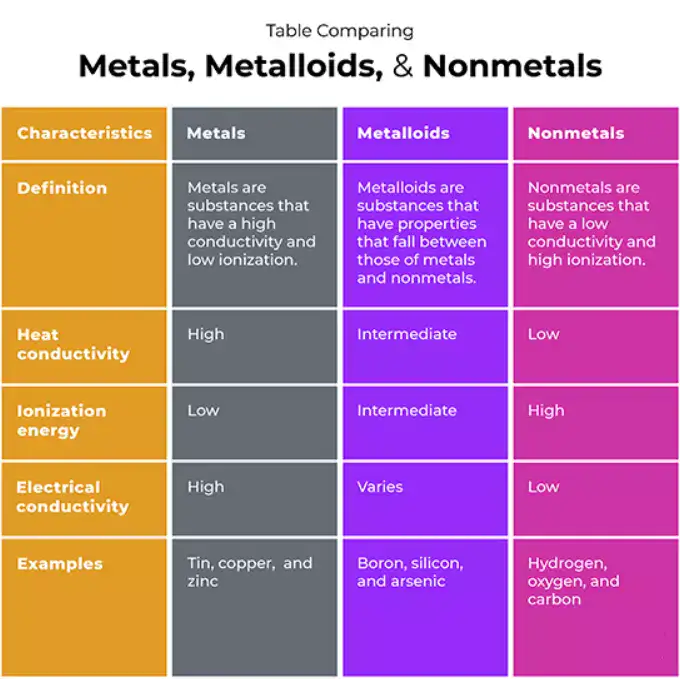
Vergleichende Tabellen - Schnellübersicht
Tabelle 1 - Physikalische und chemische Vergleiche auf hohem Niveau
| Eigenschaft / Merkmal | Metalle | Nichtmetalle | Metalloide |
|---|---|---|---|
| Typische elektrische Leitfähigkeit | Hoch | Gering bis gar nicht | Zwischenstufe / halbleitend |
| Wärmeleitfähigkeit | Hoch | Niedrig | Mäßig |
| Lüster | Metallisch (glänzend) | Stumpf / nicht metallisch | Oft metallischer Glanz |
| Mechanisches Verhalten | Duktil / verformbar (viele) | Spröde (die meisten Feststoffe) | Spröde bis halbduktil |
| Gemeinsame Oxide | Basisch / amphoterisch | sauer / kovalent | Amphoterisch |
| Typische Verklebung | Metallisch/ionisch | Kovalent / molekular | Kovalent mit teilweise metallischem Charakter |
| Regelmäßiger Standort | Links / Mitte / Unten | Rechts / oben | Treppengrenze |
Tabelle 2 - Repräsentative Beispiele und typische Verwendungen
| Kategorie | Repräsentative Elemente | Typische industrielle Anwendungen |
|---|---|---|
| Metalle | Eisen (Fe), Kupfer (Cu), Aluminium (Al), Nickel (Ni), Titan (Ti) | Baustahl, elektrische Verkabelung, Luft- und Raumfahrt, korrosionsbeständige Legierungen |
| Nichtmetalle | Sauerstoff (O), Stickstoff (N), Schwefel (S), Kohlenstoff (C), Phosphor (P) | Chemische Ausgangsstoffe, Polymere, Oxidationsmittel, Katalysatoren (Kohlenstoffträger) |
| Metalloide | Silizium (Si), Germanium (Ge), Bor (B), Antimon (Sb), Tellur (Te) | Halbleiter, Thermoelektrik, Spezialkeramiken, Legierungszusätze |
Tabelle 3 - Elektronische Signatur und Extraktionshinweise
| Element-Klasse | Verhalten von Valenzelektronen | Typische Erzquelle | Typischer Gewinnungs- oder Verarbeitungsweg |
|---|---|---|---|
| Metalle | Delokalisierte Leitungselektronen | Erze: Oxide, Sulfide | Pyrometallurgie, Hydrometallurgie, elektrolytische Raffination |
| Nichtmetalle | Elektronenlokalisierung, kovalente Netzwerke | Einheimische Gase, mineralische Ablagerungen (z. B. Schwefel), organische Quellen | Chemische Synthese, Gastrennung, Bergbau (z. B. Graphit) |
| Metalloide | Enge Bandlücke, gerichtete kovalente Bindungen | Silikate, Sulfide, native Formen | Chemische Reinigung (Zonenraffination für Si), Rösten und Auslaugen |

Geologisches Vorkommen, Gewinnung und Handelsformen
Aus Sicht der Beschaffung und Verarbeitung:
-
Metalle: Häufig aus Oxiden und Sulfidmineralien gewonnen (z. B. Hämatit für Eisen, Chalkopyrit für Kupfer). Bei der Verhüttung werden Sauerstoff oder Schwefel entfernt; durch Elektroraffination und magnetohydrometallurgische Schritte wird hochreines Metall gewonnen. Handelsformen: Barren, Knüppel, Bleche, Spulen, Draht, Pulver.
-
Nichtmetalle: Treten in elementarer, molekularer oder mineralischer Form auf. Kohlenstoff erscheint als Graphit oder Diamant; Schwefel kommt in elementaren Ablagerungen oder vulkanischen Emissionen vor; Stickstoff und Sauerstoff sind atmosphärische Gase, die durch Luftzerlegung gewonnen werden. Zu den kommerziellen Formen gehören Gase, Pulver und molekulare Feststoffe.
-
Metalloide: Silizium wird aus Quarz gewonnen und durch karbothermische Reduktion zu metallurgischem Silizium aufbereitet, das dann mit chemischen Methoden (z. B. dem Siemens-Verfahren oder Wirbelschichtreaktoren) zu elektronischem Silizium gereinigt wird. Bor wird aus Boraten gewonnen; Germanium wird häufig aus Zinkerzen oder Kohleflugasche gewonnen.
Industrielle Anwendungen und Beispiele mit praktischen Beschaffungshinweisen
Elementweise Zusammenfassungen mit Kaufüberlegungen:
-
Eisen / Stahl (Metall): Primäres Konstruktionsmetall. Die Einkaufsspezifikationen beziehen sich in der Regel auf Normen (ASTM A36, A992 usw.), und die Mikrostruktur spielt eine Rolle (z. B. ferritisch, martensitisch). Korrosionsbeständigkeit und Schweißbarkeit hängen von der Zusammensetzung und der Wärmebehandlung ab.
-
Kupfer (Metall): Entscheidend für die elektrische Leitfähigkeit. Kaufsorten (z. B. C11000, C10200) geben Reinheit und Leitfähigkeit an. Sauerstofffreies Kupfer wird verwendet, wenn hohe Leitfähigkeit und geringe Verunreinigungen erforderlich sind.
-
Aluminium (Metall): Bevorzugt dort, wo geringe Dichte und Korrosionsbeständigkeit entscheidend sind. Die Legierungsserien (1000 bis 7000) bestimmen die wichtigsten Eigenschaften. Die Oberflächenbeschaffenheit und der Härtegrad spielen eine Rolle bei der Umformung und bei strukturellen Anwendungen.
-
Silizium (Metalloid): Silizium in elektronischer Qualität wird für Wafer verwendet; Silizium in metallurgischer Qualität wird für Legierungen und Silikone verwendet. Beim Einkauf muss auf die Reinheit geachtet werden (ppb-Werte für Elektronik).
-
Kohlenstoff (Nicht-Metall): Graphit wird als Hochtemperaturelektrode und Schmiermittel verwendet; Aktivkohle für die Adsorption. Form und Porosität bestimmen die Leistung.
Beschaffungstipp: Fordern Sie Materialzertifikate an (Werksprüfberichte, chemische und mechanische Prüfberichte), bestätigen Sie die Grenzwerte für Spurenverunreinigungen bei kritischen Anwendungen, und überprüfen Sie die Einhaltung der geltenden Normen (ASTM, ISO, EN).
Legierung, Behandlung und Eigenschaftsänderung
Wie sich die Unterschiede auf gängige industrielle Prozesse übertragen lassen:
-
Legierungsmetalle: Die Beimischung von Elementen verändert die Elektronendichte, die Gitterverzerrung und die Phasenstabilität. So bildet beispielsweise Kohlenstoff in Eisen Stahl mit drastisch erhöhter Festigkeit; Chrom erhöht die Korrosionsbeständigkeit in rostfreien Stählen.
-
Dotierung von Metalloiden: Die kontrollierte Einführung von Donor- oder Akzeptor-Verunreinigungen wandelt intrinsische Halbleiter in n- oder p-Typen um, was das elektrische Verhalten bestimmt. Temperatur und Konzentration regulieren die Mobilität der Ladungsträger.
-
Funktionalisierung von Nichtmetallen: Nichtmetalle bilden funktionelle Verbindungen (z. B. Kohlenstoff in Polymeren, Schwefel in vulkanisiertem Gummi), die bestimmte chemische oder mechanische Eigenschaften aufweisen.
-
Wärmebehandlung: Metalle reagieren gut auf Glühen, Abschrecken, Anlassen und Aushärten. Metalloide und nichtmetallische Werkstoffe erfordern spezielle thermische oder chemische Verfahren zur Eigenschaftsanpassung (z. B. Sintern von Keramik, Glühen von Glas).
Sicherheit, Handhabung und Umweltaspekte
Praktische Sicherheitspunkte für jede Klasse:
-
Metalle: Viele Metalle erzeugen beim Schneiden, Schweißen oder Schmelzen giftige Stäube oder Dämpfe (z. B. Blei, Cadmium). Korrodierte Metalle können gefährliche Nebenprodukte erzeugen. Verwenden Sie geeignete PSA und Belüftung und halten Sie die Abfallentsorgungsvorschriften ein.
-
Nichtmetalle: Reaktive Nichtmetalle (z. B. Phosphor, Chlorgas) stellen eine akute Gefahr dar; Pulver (z. B. Ruß) können eine Staubexplosionsgefahr darstellen. Befolgen Sie die MSDS-Anleitung.
-
Metalloide: Einige Metalloide sind toxikologisch bedenklich (z. B. Arsenverbindungen). Halbleitermaterialien können eine Kontaminationskontrolle und eine Handhabung im Reinraum erfordern.
-
Umwelt: Die Auswirkungen über den gesamten Lebenszyklus sind sehr unterschiedlich: Metalle sind oft mit einer energieintensiven Gewinnung verbunden, während die Herstellung einiger Nichtmetalle (wie z. B. aus der Petrochemie gewonnene Polymere) andere Schadstoffprofile aufweist. Recycling- und Substitutionsüberlegungen spielen bei der Beschaffungsstrategie eine wichtige Rolle.
Wie man eine unbekannte Probe im Labor oder in der Werkstatt identifiziert
Ein schrittweises praktisches Protokoll:
-
Sichtprüfung: Achten Sie auf Farbe, Glanz und Textur. Metallischer Glanz deutet auf Metall oder Metalloid hin.
-
Messung der Dichte: Die durch Verdrängung gemessene Schüttdichte ist ein wichtiger Anhaltspunkt. Eine hohe Dichte deutet auf Metall hin (aber prüfen Sie auf schwere Nichtmetalle wie Jod).
-
Elektrischer Test: Verwenden Sie ein Multimeter zur Messung der Gleichstromleitfähigkeit. Eine hohe Leitfähigkeit deutet auf ein Metall hin, eine niedrige auf ein Nichtmetall, ein temperaturabhängiges Zwischenverhalten auf ein Metalloid/Halbleiter.
-
Mechanische Prüfung: Einfache Biege- oder Kratztests zeigen Duktilität bzw. Sprödigkeit an. Metalle verformen sich in der Regel, Nichtmetalle zerbrechen oft.
-
Chemische Stichprobentests: Durch die Reaktion kleiner Proben mit Säuren oder durch Flammentests kann das Klassenverhalten ermittelt werden - Metalle können sich auflösen und farbige Ionen bilden; Nichtmetalle bilden Gase oder unlösliche Rückstände. Befolgen Sie stets die Sicherheitsprotokolle.
-
Spektroskopische Bestätigung: XRF, AES, ICP-MS oder XRD liefern die endgültige Zusammensetzung und Phasenidentifikation für die Überprüfung der Beschaffungsqualität.
FAQs
Q1: Welcher grundlegende elektronische Unterschied unterscheidet Metalle von Nichtmetallen?
A: Metalle verfügen über delokalisierte Valenzelektronen, die Leitungsbänder bilden und die Bewegung freier Elektronen unter einem elektrischen Feld ermöglichen. Nichtmetalle haben lokalisierte Elektronen, die gefüllte oder fast gefüllte Valenzschalen besetzen, die gerichtete kovalente Bindungen unterstützen und zu einer schlechten elektrischen Leitfähigkeit in der Masse führen.
F2: Sind Metalloide immer Halbleiter?
A: Nicht immer. Viele Metalloide haben ein intrinsisches halbleitendes Verhalten mit schmalen Bandlücken (Beispiel: Silizium, Germanium), aber physikalische Form, Dotierung und Temperatur beeinflussen die Leitfähigkeit stark; einige Metalloide verhalten sich in bestimmten kristallinen Morphologien metallischer.
F3: Wie spiegeln die Oxideigenschaften die Elementklassifizierung wider?
A: Metalloxide sind in der Regel basisch oder amphoter, neutralisieren Säuren und bilden Salze. Nichtmetalloxide sind in der Regel sauer und bilden in Wasser Säuren (z. B. SO₂ → schweflige Säure). Metalloide bilden in der Regel amphotere Oxide, die sowohl basisch als auch sauer reagieren.
F4: Mit welchen Tests lässt sich schnell feststellen, ob ein Metall ein Übergangsmetall oder ein Hauptgruppenmetall ist?
A: Übergangsmetalle weisen in der Regel mehrere stabile Oxidationsstufen, farbige Ionen in Lösung und ein komplexes Bildungsverhalten auf; Metalle der Hauptgruppe weisen in der Regel weniger Oxidationsstufen und einfachere binäre Verbindungen auf.
F5: Wie wichtig ist die Reinheit von Industriesilizium für die Elektronik?
A: Äußerst wichtig. Silizium in Elektronikqualität erfordert Verunreinigungsgrade im ppb-Bereich oder darunter; Spurenmetalle können die Lebensdauer der Ladungsträger und die Ausbeute der Bauelemente drastisch verändern.
F6: Können Nichtmetalle Legierungen bilden?
A: Nicht im klassischen metallischen Sinne. Allerdings verbinden sich nichtmetallische Elemente zu Mischungen und Verbundwerkstoffen (z. B. Kohlenstoff in graphitverstärkten Verbundwerkstoffen oder Polymermischungen), die in bestimmten Anwendungen legierungsähnliche Funktionen erfüllen.
F7: Welche Klasse korrodiert am leichtesten und wie wird der Schutz erreicht?
A: Die Korrosionsneigung hängt von der Umgebung und dem Element ab: Eisen rostet leicht in feuchtem Sauerstoff; viele Nichtmetalle korrodieren nicht, können aber oxidieren oder sich zersetzen. Zu den Schutzmethoden gehören Beschichtungen, kathodischer Schutz, Legierung und Umweltkontrolle.
F8: Gibt es Elemente, die sich einer einfachen Klassifizierung entziehen?
A: Ja. Mehrere Elemente liegen nahe der Metalloidgrenze und zeigen Polymorphismus mit sowohl metallischen als auch nichtmetallischen Phasen. Außerdem können Elemente unter extremem Druck oder Temperatur ihr Verhalten ändern.
F9: Wie beeinflussen Legierungszusätze von Metalloiden die Metalleigenschaften?
A: Kleine Zusätze von Metalloiden (z. B. Silizium, Bor) verfeinern die Korngröße, verändern die Härtbarkeit, verbessern die Festigkeit bei Temperatur oder verändern das elektrische Verhalten. Silizium in Stahl beeinflusst beispielsweise die Desoxidation und die magnetischen Eigenschaften.
Q10: Welche Werkstoffnormen sollten bei der Spezifikation von Metallen für die Beschaffung herangezogen werden?
A: Zu den gängigen Normen gehören ASTM (amerikanisch), EN (europäisch), ISO, JIS (japanisch), je nach Region. Für elektronische Materialien gelten die JEDEC- und halbleiterspezifischen Normen. Fordern Sie stets einschlägige Werksprüfberichte und Konformitätsdokumente an.
Maßgebliche Referenzen
- IUPAC - Periodensystem und Elementinformationen
- NIST Chemistry WebBook - Thermochemische und spektroskopische Daten
- Royal Society of Chemistry - Interaktives Periodensystem und Elementdaten
- USGS - Informationen über Metalle und Mineralien (National Minerals Information Center)
Schlussbemerkungen und empfohlene nächste Schritte
-
Für die Beschaffungsdokumentation sollten Sie dieses konzeptionelle Material mit den geltenden ASTM/EN-Normen für jedes spezifische Metall oder jede Legierung verbinden.
-
Wenn Sie Lehrmaterial oder Webinhalte vorbereiten, wandeln Sie die Tabellen in responsives HTML mit Mikrodaten um, um bessere Suchmaschinenergebnisse zu erzielen.
-
Wenn Sie weitere Einzelheiten zu einem einzelnen Element, einem Legierungssystem oder einer Verarbeitungsmethode benötigen (z. B. Wärmebehandlungspläne für bestimmte Stähle, Reinheitsgrade von Siliziumwafern oder Korrosionsprüfungsdaten), geben Sie den Namen des Elements oder der Legierung und die beabsichtigte Anwendung an; dann kann eine gezielte technische Beschreibung erstellt werden.

