المعادن هي العناصر التي عادةً ما تكون موصلة للكهرباء والحرارة، وتُظهر بريقًا فلزيًّا، وتتشوه بشكل مرن تحت الضغط، وتتخلى عن الإلكترونات في التفاعلات الكيميائية؛ أما اللافلزات فهي عادةً ما تفتقر إلى البريق الفلزي، وهي موصِّلات كهربائية ضعيفة، وتميل إلى اكتساب الإلكترونات أو مشاركتها وتكوين أكاسيد تساهمية أو حمضية؛ وتُظهر أشباه الفلزات سلوكًا هجينًا، حيث تمتلك مزيجًا من الخواص الفلزية واللافلزية التي تجعلها ذات قيمة في أشباه الموصلات والسبائك المتخصصة.
التصنيف التاريخي والأساس المنطقي
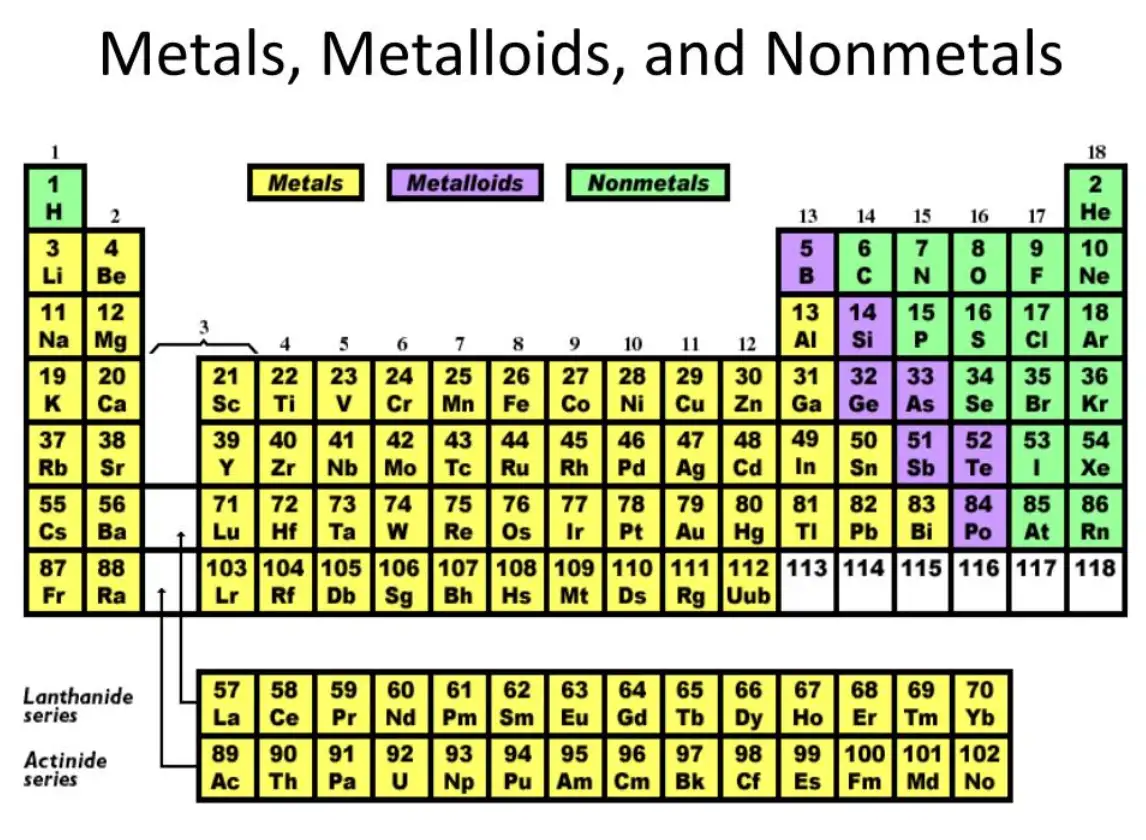
يعود تاريخ تصنيف العناصر إلى فلزات ولا فلزات إلى بدايات الكيمياء وعلم المعادن عندما كانت خواص مثل قابلية الطرقة واللمعان والقدرة على تكوين السبائك هي سمات الفرز الأساسية. أدى تطور الجدول الدوري إلى تنقيح النظام: المجموعات الموجودة على اليسار والوسط هي في الغالب فلزات في الغالب، والمجموعات الموجودة على اليمين هي لا فلزية إلى حد كبير، مع وجود شريط قطري ضيق من العناصر التي تظهر سمات مختلطة: أشباه الفلزات. وشملت القوى الدافعة العملية للتصنيف: المنفعة المعدنية، وسهولة الاستخراج، والأهمية الاقتصادية، والسلوك الكيميائي التنبؤي. في الممارسة الحديثة، يدعم التصنيف اختيار المواد وتصميم العمليات والنمذجة التنبؤية.
تحديد الخصائص: المعايير الفيزيائية
قائمة مرجعية فنية مفيدة أثناء تحديد الهوية:
-
التوصيل الكهربائي: مرتفعة في معظم الفلزات بسبب وجود بحر من الإلكترونات غير المتمركزة. منخفضة في معظم اللافلزات. غالبًا ما تُظهر أشباه الفلزات موصلية شبه موصلة تتغير بشدة مع درجة الحرارة والتطعيم.
-
التوصيل الحراري: المعادن عادةً ما تقوم المعادن بتوصيل الحرارة بكفاءة؛ أما اللافلزات فتوصيلها الحراري أضعف؛ وتختلف الفلزات.
-
اللمعان والانعكاسية: تُظهر الفلزات بريقًا معدنيًا مميزًا وانعكاسية عالية على الأسطح المصقولة، بينما تكون العديد من اللافلزات باهتة أو شفافة، وغالبًا ما تُظهر الفلزات لمعانًا معدنيًا خافتًا.
-
المرونة والليونة: تتشوه الفلزات تشوهًا بلاستيكيًا تحت ضغط يسمح بالدرفلة أو التشكيل أو السحب؛ أما اللافلزات فهي هشة في شكلها الصلب السائب؛ وقد تكون الفلزات هشة ولكن يمكن تشغيلها أحيانًا في ظروف متخصصة.
-
القوة الميكانيكية: تمتد المعادن على نطاق واسع من المعادن اللينة (مثل الصوديوم) إلى القوية للغاية (مثل الفولاذ عالي القوة)؛ ويعتمد الأداء الميكانيكي بشكل كبير على البنية المجهرية والسبائك.
-
الكثافة: تتميز المعادن عمومًا بكثافة أعلى من اللافلزات، على الرغم من وجود استثناءات (على سبيل المثال، اليود اللافلزي الكثيف).
-
المرحلة عند STP (درجة الحرارة والضغط القياسيين): معظم الفلزات صلبة عند STP (الزئبق استثناء سائل مهم). أما اللافلزات فقد تكون غازات (O₂، N₂) أو سوائل (البروم) أو مواد صلبة (الكربون والكبريت).
تحديد الخواص: السلوك الكيميائي وميول الترابط الكيميائي
تنشأ الاختلافات الكيميائية من السالبية الكهربية وطاقة التأين وتقارب الإلكترونات:
-
الميل إلى فقدان الإلكترونات: للفلزات طاقات تأيُّن منخفضة نسبيًّا وتشكل الكاتيونات بسهولة. وتشكل روابط أيونية مع العديد من اللافلزات والروابط الفلزية في شكلها النقي أو السبائك.
-
الميل إلى اكتساب أو مشاركة الإلكترونات: اللافلزات لها سالبية كهربية وطاقات تأين أعلى، مما يفضل اكتساب الإلكترونات أو مشاركتها ؛ فهي تشكل شبكات تساهمية أو جزيئات ثنائية الذرة أو أنيونات متعددة الذرات.
-
طابع الأكسيد: تميل أكاسيد الفلزات إلى أن تكون قاعدية أو مذبذبة، في حين أن أكاسيد اللافلزات غالبًا ما تكون حمضية؛ وقد تشكل أكاسيد الفلزات أكاسيد مذبذبة تظهر كلا السلوكين اعتمادًا على الشريك المتفاعل.
-
سلوك الأكسدة والاختزال في البيئات النموذجية: تعمل الفلزات كعوامل مختزلة عند التلامس مع البيئات الحمضية؛ وغالبًا ما تعمل اللافلزات على أكسدة الفلزات أو تعمل كمؤكسدات عند الاقتضاء.
-
التكوين المعقد: تُكوِّن الفلزات الانتقالية معقدات تناسقية بسهولة بسبب المشاركة المدارية d، بينما تشارك اللافلزات والفلزات بشكل مختلف في الكيمياء المعقدة.
التركيب الإلكتروني والوضع الدوري
يوضح فهم مكان ظهور كل فئة في الجدول الدوري كلاً من الاتجاهات والاستثناءات:
-
المعادن: تشغل الكتلة s، والكتلة d، والكتلة f، وجزء من الكتلة p. تتميز بنطاقات توصيل مملوءة جزئيًا ووظائف عمل منخفضة. تُظهر الفلزات الانتقالية (المربع d) حالات أكسدة متغيرة وخصائص مغناطيسية وحفازة معقدة.
-
اللافلزات: التجمع نحو أعلى يمين الجدول الدوري (باستثناء الغازات النبيلة في فئة منفصلة). ينتج عن أنصاف الأقطار الذرية الصغيرة، والسالبية الكهربية العالية، وأغلفة التكافؤ المملوءة أو شبه المملوءة ترابط اتجاهي قوي.
-
الفلزات: تقع على الدرج المتدرج بين الفلزات واللافلزات: البورون والسيليكون والجرمانيوم والزرنيخ والأنتيمون والتيلوريوم والبولونيوم (تختلف التصنيفات). تخلق هياكل نطاقاتها فجوات نطاق ضيقة مناسبة لتطبيقات أشباه الموصلات.
أشباه الفلزات: التعريف، والتعريف، والسلوك الحدّي
تستحق الفلزات اهتمامًا خاصًا لأن خصائصها الوسيطة تدعم الإلكترونيات الحديثة والسبائك المتخصصة:
-
أشباه المعادن الكنسية: البورون (B)، والسيليكون (Si)، والجرمانيوم (Ge)، والزرنيخ (As)، والأنتيمون (Sb)، والتيلوريوم (Te). البولونيوم مدرج أحيانًا ولكن له اعتبارات إشعاعية.
-
سبب أهمية الفلزات ويمكن ضبط سلوكها شبه الموصّل عن طريق التطعيم ودرجة الحرارة؛ كما أنها تشكل أطوارًا زجاجية وسيراميك مع اللافلزات؛ وتعمل كعناصر إشابة تعدل الخواص الميكانيكية والحرارية.
-
الأشكال الهيكلية: وتشكل العديد من الفلزات شبكات تساهمية (مثل السيليكون) تكون هشة ولكنها نشطة كهربائيًا عند تخديرها. والبعض الآخر (على سبيل المثال، الأنتيمون) لها هياكل بلورية متعددة الطبقات تُظهر سلوكًا متباين الخواص.
-
الدور الصناعي: أشباه الموصلات (سيليكون، جي)، ومثبطات اللهب ومعدلات السبائك (Sb)، والمواد الكهروحرارية (Te)، والسيراميك المتخصص (B).
جداول المقارنة - مرجع سريع
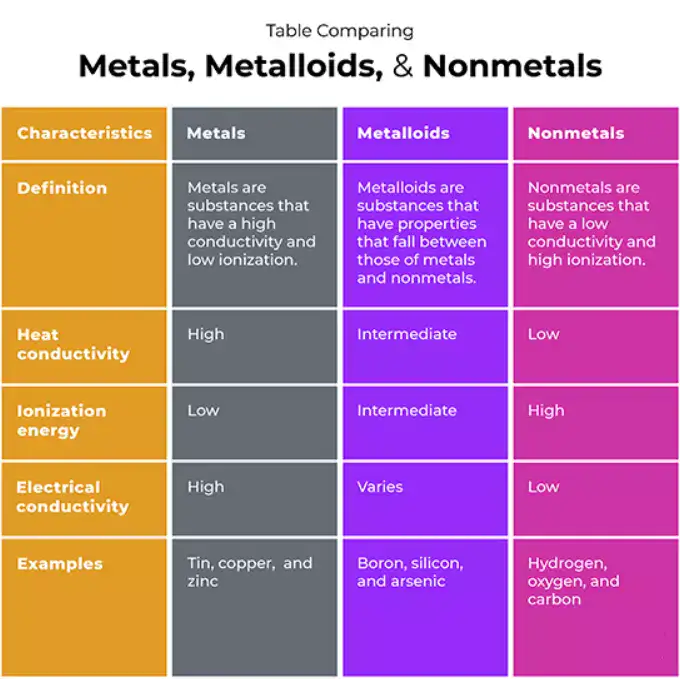
الجدول 1 - مقارنة فيزيائية وكيميائية عالية المستوى
| الملكية / الميزة | المعادن | اللافلزات | الفلزات |
|---|---|---|---|
| التوصيل الكهربائي النموذجي | عالية | منخفضة إلى معدومة | وسيطة/شبه موصلة |
| التوصيل الحراري | عالية | منخفضة | معتدل |
| اللمعان | معدني (لامع) | باهتة/غير معدنية | لمعان معدني في كثير من الأحيان |
| السلوك الميكانيكي | مطاطي/مرن (كثير) | هش (معظم المواد الصلبة) | هش إلى شبه هش |
| الأكاسيد الشائعة | أساسي / أمفوتيريك | حمضي / تساهمي | أمفوتيريك |
| الترابط النموذجي | معدني/أيوني | التساهمي / الجزيئي | تساهمية ذات طابع فلزي جزئي معدني |
| الموقع الدوري | يسار/وسط/أسفل | اليمين/الأعلى | حدود السلالم المتدرجة |
الجدول 2 - أمثلة تمثيلية واستخدامات نموذجية
| الفئة | العناصر التمثيلية | الاستخدامات الصناعية النموذجية |
|---|---|---|
| المعادن | الحديد (Fe) والنحاس (Cu) والألومنيوم (Al) والنيكل (Ni) والتيتانيوم (Ti) | الفولاذ الإنشائي، والأسلاك الكهربائية، والفضاء، والسبائك المقاومة للتآكل |
| اللافلزات | الأكسجين (O)، والنيتروجين (N)، والكبريت (S)، والكربون (C)، والفوسفور (P) | المواد الأولية الكيميائية، والبوليمرات، والمؤكسدات، والمحفزات (دعامات الكربون) |
| الفلزات | السيليكون (Si)، والجرمانيوم (Ge)، والبورون (B)، والأنتيمون (Sb)، والتيلوريوم (Te) | أشباه الموصلات، والكهرباء الحرارية، والسيراميك الخاص، والمواد المضافة إلى السبائك |
الجدول 3 - التوقيع الإلكتروني/التوقيع الإلكتروني/الترابط وملاحظات الاستخراج
| فئة العنصر | سلوك إلكترون التكافؤ | مصدر الخام النموذجي | مسار الاستخراج أو المعالجة النموذجي |
|---|---|---|---|
| المعادن | إلكترونات التوصيل غير المتمركزة | الخامات: الأكاسيد، الكبريتيدات | علم المعادن الحراري، علم المعادن المائي، التكرير الإلكتروليتي |
| اللافلزات | توطين الإلكترونات، الشبكات التساهمية | الغازات المحلية، والرواسب المعدنية (مثل الكبريت)، والمصادر العضوية | التخليق الكيميائي، فصل الغاز، التعدين (مثل الجرافيت) |
| الفلزات | فجوة النطاق الضيقة، الروابط التساهمية الاتجاهية | السيليكات، الكبريتيدات، الأشكال الأصلية | تنقية كيميائية (تنقية المنطقة من السيليكون)، والتحميص والرشح |

التواجد الجيولوجي والاستخراج والأشكال التجارية
من وجهة نظر المشتريات والمعالجة:
-
المعادن: كثيرًا ما يتم تعدينها من الأكاسيد ومعادن الكبريتيد (مثل الهيماتيت للحديد، والكالكوبيرايت للنحاس). ويؤدي الصهر إلى إزالة الأكسجين أو الكبريت؛ وتنتج خطوات التكرير الكهربائي والمعدن المغناطيسي الهيدروجيني معدنًا عالي النقاء. الأشكال التجارية: سبائك، قضبان، صفائح، لفائف، أسلاك، مسحوق.
-
اللافلزات: تحدث في أشكال عنصرية أو جزيئية أو معدنية. يظهر الكربون في شكل جرافيت أو ماس؛ ويوجد الكبريت في رواسب عنصري أو انبعاثات بركانية؛ أما النيتروجين والأكسجين فهما غازان في الغلاف الجوي يتم الحصول عليهما عن طريق فصل الهواء. وتشمل الأشكال التجارية الغازات والمساحيق والمواد الصلبة الجزيئية.
-
الفلزات: يتم استخلاص السيليكون من الكوارتز وتنقيته إلى سيليكون من الدرجة المعدنية عن طريق الاختزال الكربوهيدراتي، ثم تنقيته بالطرق الكيميائية (على سبيل المثال، عملية سيمنز أو مفاعلات الطبقة المميعة) للحصول على سيليكون من الدرجة الإلكترونية. ويتم الحصول على البورون من البورات؛ وغالباً ما يتم استخلاص الجرمانيوم من خامات الزنك أو الرماد المتطاير من الفحم.
استخدامات وأمثلة صناعية مع ملاحظات عملية للمشتريات
ملخصات كل عنصر على حدة مع اعتبارات الشراء:
-
حديد/فولاذ (معدن): المعدن الإنشائي الأساسي. عادةً ما تشير مواصفات الشراء عادةً إلى المعايير المرجعية (ASTM A36، A992، إلخ)، كما أن البنية المجهرية مهمة (على سبيل المثال، الحديدي والمارتنسيتي). تعتمد مقاومة التآكل وقابلية اللحام على التركيب والمعالجة الحرارية.
-
نحاس (معدن): حاسم للتوصيل الكهربائي. تشير درجات الشراء (مثل C11000، C10200) إلى النقاء والتوصيل. يُستخدم النحاس الخالي من الأكسجين حيثما تكون الموصلية العالية ومستويات الشوائب المنخفضة مطلوبة.
-
ألومنيوم (معدن): مفضلة في الحالات التي تكون فيها الكثافة المنخفضة ومقاومة التآكل أمران حيويان. تحدد سلسلة السبائك (من 1000 إلى 7000) الخصائص الرئيسية. تعتبر الطلاء السطحي والمزاج مهمين في تطبيقات التشكيل مقابل التطبيقات الإنشائية.
-
السيليكون (معدن السيليكون): السيليكون من الدرجة الإلكترونية المستخدم في الرقائق؛ السيليكون من الدرجة المعدنية المستخدم في السبائك والسيليكون. يتطلب الشراء اهتماماً دقيقاً بالنقاء (مستويات جزء في البليون للإلكترونيات).
-
الكربون (اللافلزات): الجرافيت المستخدم كقطب كهربائي عالي الحرارة ومواد تشحيم؛ الكربون المنشط للامتصاص. تتحكم الأشكال والمسامية في الأداء.
نصيحة المشتريات: اطلب شهادات المواد (تقارير اختبار المطاحن وتقارير الاختبارات الكيميائية والميكانيكية)، وتأكد من حدود الشوائب النزرة للتطبيقات الحرجة، وتحقق من الامتثال للمعايير المعمول بها (ASTM، ISO، EN).
السبائك، والمعالجة، وتعديل الخصائص
كيف تتوافق الاختلافات مع العمليات الصناعية شائعة الاستخدام:
-
معادن السبائك: يؤدي دمج العناصر إلى تغيير كثافة الإلكترون وتشويه الشبكة واستقرار الطور. على سبيل المثال، يشكل الكربون في الحديد فولاذًا ذا قوة متزايدة بشكل كبير؛ ويضيف الكروم مقاومة للتآكل في الفولاذ المقاوم للصدأ.
-
تخدير الفلزات المنشطات: ويؤدي الإدخال المتحكم فيه للشوائب المانحة أو المستقبلة إلى تحويل أشباه الموصلات الجوهرية إلى نوع n أو نوع p، وهو ما يملي السلوك الكهربائي. تنظم درجة الحرارة والتركيز حركة الناقل.
-
توظيف اللافلزات: وتشكل اللافلزات مركبات وظيفية (مثل الكربون في البوليمرات، والكبريت في المطاط المفلكن) التي توفر أداءً كيميائيًا أو ميكانيكيًا محددًا.
-
المعالجة الحرارية: تستجيب الفلزات بشكل جيد للتلدين والتبريد والتبريد والتلطيف والتصلب مع تقدم العمر. وتتطلب الفلزات والمواد اللافلزية طرقًا حرارية أو كيميائية متخصصة لضبط الخصائص (على سبيل المثال، تلبيد السيراميك وتلدين الزجاج).
اعتبارات السلامة والمناولة والاعتبارات البيئية
نقاط السلامة العملية لكل فئة:
-
المعادن: تنتج العديد من المعادن غبارًا أو أبخرة سامة أثناء القطع أو اللحام أو الصهر (مثل الرصاص والكادميوم). يمكن أن تنتج المعادن المتآكلة منتجات ثانوية خطرة. استخدم معدات الوقاية الشخصية المناسبة والتهوية واستيفاء قواعد التخلص من النفايات.
-
اللافلزات: تشكل اللافلزات التفاعلية (مثل الفوسفور وغاز الكلور) مخاطر حادة؛ يمكن أن تشكل المساحيق (مثل أسود الكربون) مخاطر انفجار الغبار. اتبع إرشادات MSDS.
-
الفلزات: بعض الفلزات لها مخاوف من السمية (مثل مركبات الزرنيخ). قد تتطلب المواد شبه الموصلة من الدرجة شبه الموصلة التحكم في التلوث والمناولة في غرف نظيفة.
-
البيئة: وتختلف تأثيرات دورة الحياة اختلافًا كبيرًا؛ فغالبًا ما تنطوي المعادن على استخراج كثيف للطاقة، في حين أن بعض إنتاج المواد غير المعدنية (مثل البوليمرات المشتقة من البتروكيماويات) ينطوي على ملامح ملوثة مختلفة. وتؤدي اعتبارات إعادة التدوير والإحلال دوراً رئيسياً في استراتيجية الشراء.
كيفية التعرف على عينة مجهولة في المختبر أو ورشة العمل
بروتوكول عملي تدريجي:
-
الفحص البصري: لاحظ اللون واللمعان والملمس. يشير اللمعان المعدني إلى معدن أو معدن معدني.
-
قياس الكثافة: تعطي الكثافة السائبة المقاسة بالإزاحة دليلًا قويًا. تشير الكثافة العالية إلى وجود فلز (ولكن تحقق من اللافلزات الثقيلة مثل اليود).
-
اختبار كهربائي: استخدم مقياس متعدد لقياس توصيلية التيار المستمر. تشير الموصلية العالية إلى وجود فلز؛ وتشير الموصلية المنخفضة إلى وجود لا فلز؛ ويشير السلوك المتوسط المعتمد على درجة الحرارة إلى وجود فلز/شبه موصل.
-
اختبار ميكانيكي: تشير اختبارات الثني أو الخدش البسيطة إلى الليونة مقابل الهشاشة. عادةً ما تتشوه المعادن؛ أما اللافلزات فغالباً ما تنكسر.
-
اختبارات البقع الكيميائية: يمكن أن يؤدي تفاعل العينات الصغيرة مع الأحماض أو استخدام اختبارات اللهب إلى تحديد سلوك الفئة - قد تذوب المعادن لتكوين أيونات ملونة؛ بينما تنتج اللافلزات غازات أو مخلفات غير قابلة للذوبان. اتبع دائمًا بروتوكولات السلامة.
-
التأكيد الطيفي: يوفر XRF أو AES أو ICP-MS أو XRD التركيب النهائي وتحديد الطور للتحقق من درجة المشتريات.
الأسئلة الشائعة
س1: ما الفرق الإلكتروني الأساسي الذي يفصل بين الفلزات واللافلزات؟
A: وتمتلك الفلزات إلكترونات تكافؤ غير متمركزة تشكل نطاقات توصيل، مما يتيح حركة الإلكترونات الحرة تحت مجال كهربائي. وتحتوي اللافلزات على إلكترونات موضعية تشغل أغلفة تكافؤ مملوءة أو شبه مملوءة، مما يدعم الروابط التساهمية الاتجاهية ويؤدي إلى ضعف التوصيل الكهربائي في الجزء الأكبر.
س2: هل أشباه الموصِّلات الفلزية دائمًا أشباه موصِّلات؟
A: ليس دائمًا. فالعديد من أشباه الفلزات لها سلوك شبه موصل جوهري مع وجود فجوات ضيقة النطاق (على سبيل المثال: السيليكون والجرمانيوم)، ولكن الشكل الفيزيائي والتخدير ودرجة الحرارة تؤثر بشدة على التوصيلية؛ فبعض أشباه الفلزات تتصرف بشكل فلزي أكثر في أشكال بلورية معينة.
س3: كيف تعكس خواص الأكسيد تصنيف العناصر؟
A: أكاسيد الفلزات عادةً ما تكون قاعدية أو مذبذبة، حيث تعمل على معادلة الأحماض لتكوين أملاح. وعادةً ما تكون الأكاسيد اللافلزية حمضية، وتشكل الأحماض في الماء (على سبيل المثال، SO₂ → حمض الكبريت). عادةً ما تشكل الفلزات عادةً أكاسيد مذبذبة مع تفاعلات قاعدية وحمضية.
س4: ما الاختبارات التي تُحدِّد بسرعة إذا ما كان الفلز فلزًّا انتقاليًّا أو فلزًّا من المجموعة الرئيسية؟
A: تُظهِر الفلزات الانتقالية عادةً حالات أكسدة متعددة مستقرة، وأيونات ملونة في المحلول، وسلوك تكوين معقد؛ وعادةً ما تُظهِر فلزات المجموعة الرئيسية حالات أكسدة أقل ومركبات ثنائية أبسط.
س5: ما مدى أهمية النقاء بالنسبة للسيليكون الصناعي المستخدم في الإلكترونيات؟
A: مهم للغاية. يتطلب السيليكون من الدرجة الإلكترونية مستويات شوائب في نطاق الأجزاء من المليار (جزء في المليار) أو أقل؛ حيث يمكن أن تغير المعادن النزرة بشكل كبير من عمر الناقل وإنتاجية الجهاز.
س6: هل يمكن أن تُكوِّن اللافلزات سبائك؟
A: ليس بالمعنى المعدني الكلاسيكي. ومع ذلك، فإن العناصر اللافلزية تتحد لتكوين مخاليط ومركبات (على سبيل المثال، الكربون في مركبات معززة بالجرافيت أو خلائط البوليمر) التي تؤدي أدوارًا شبيهة بالسبائك في بعض التطبيقات.
س7: ما هي الفئة التي تتآكل بسهولة أكبر وكيف يتم تحقيق الحماية؟
A: يعتمد الميل إلى التآكل على البيئة والعنصر: يصدأ الحديد بسهولة في الأكسجين الرطب؛ العديد من اللافلزات لا تتآكل ولكن يمكن أن تتأكسد أو تتحلل. تشمل طرق الحماية الطلاءات والحماية الكاثودية وإضافة السبائك والتحكم البيئي.
س 8: هل هناك عناصر تتحدى التصنيف البسيط؟
A: نعم، تقع عدة عناصر بالقرب من حدود الفلزات وتُظهِر تعدد الأشكال مع كل من الأطوار الفلزية واللافلزية. بالإضافة إلى ذلك، قد تغير العناصر تحت الضغط الشديد أو درجة الحرارة القصوى سلوكها.
س9: كيف تؤثر إضافات السبائك للفلزات على خواص الفلزات؟
A: تعمل الإضافات الصغيرة من الفلزات (مثل السيليكون والبورون) على تحسين حجم الحبيبات أو تغيير الصلابة أو تحسين القوة عند درجة الحرارة أو تغيير السلوك الكهربائي. على سبيل المثال، يؤثر السيليكون في الفولاذ على إزالة الأكسدة والخصائص المغناطيسية.
Q10: ما هي معايير المواد التي ينبغي الرجوع إليها عند تحديد مواصفات المعادن للمشتريات؟
A: تشمل المعايير الشائعة ASTM (الأمريكية) وEN (الأوروبية) وISO وJIS (اليابانية) حسب المنطقة. بالنسبة للمواد الإلكترونية، تنطبق معايير JEDEC والمعايير الخاصة بأشباه الموصلات. اطلب دائمًا تقارير اختبار المطاحن ذات الصلة ووثائق الامتثال.
مراجع موثوقة
- IUPAC - الجدول الدوري ومعلومات العناصر
- الكتاب الإلكتروني للكيمياء التابع للمعهد الوطني للمعايير والتكنولوجيا النووية - البيانات الكيميائية الحرارية والطيفية
- الجمعية الملكية للكيمياء - الجدول الدوري التفاعلي وبيانات العناصر
- هيئة المسح الجيولوجي الأمريكية - معلومات عن المعادن والفلزات (المركز الوطني للمعلومات عن المعادن)
الملاحظات الختامية والخطوات التالية الموصى بها
-
بالنسبة لوثائق المشتريات، قم بإقران هذه المادة المفاهيمية بمعايير ASTM/EN المعمول بها لكل معدن أو سبيكة محددة.
-
بالنسبة للأشخاص الذين يعدون المواد التعليمية أو محتوى الويب، قم بتحويل الجداول إلى HTML متجاوب مع البيانات المصغرة للحصول على نتائج أغنى لمحرك البحث.
-
إذا كانت هناك حاجة إلى مزيد من التفاصيل عن أي عنصر واحد أو نظام سبيكة أو مسار معالجة (على سبيل المثال، جداول المعالجة الحرارية لأنواع محددة من الفولاذ أو مسارات نقاء رقائق السيليكون أو بيانات اختبار التآكل)، قدم اسم العنصر أو السبيكة والتطبيق المقصود؛ ويمكن بعد ذلك إعداد موجز فني مستهدف.

