Los metales son elementos que suelen conducir la electricidad y el calor, presentan brillo metálico, se deforman plásticamente bajo tensión y ceden electrones en las reacciones químicas; los no metales suelen carecer de brillo metálico, son malos conductores eléctricos, tienden a ganar o compartir electrones y forman óxidos covalentes o ácidos; los metaloides presentan un comportamiento híbrido, ya que poseen una mezcla de propiedades metálicas y no metálicas que los hacen valiosos en semiconductores y aleaciones especializadas.
Clasificación histórica y justificación
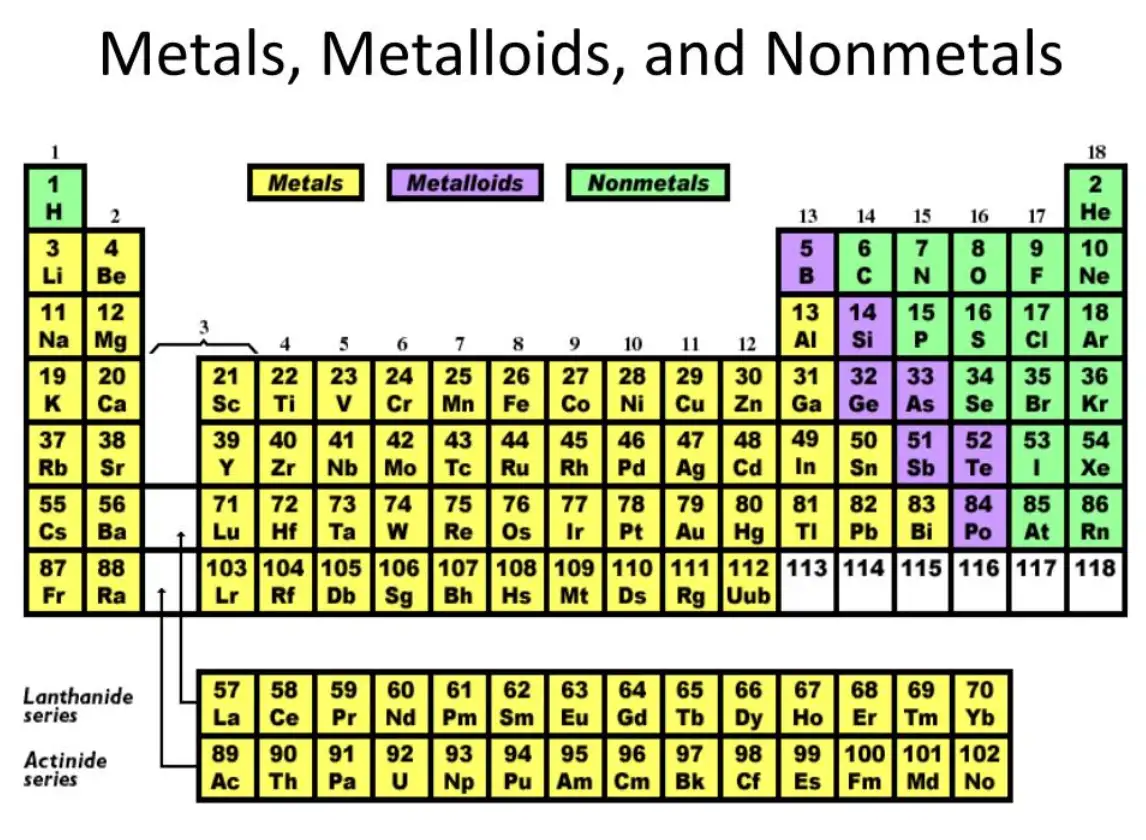
La clasificación de los elementos en metales y no metales se remonta a los orígenes de la química y la mineralogía, cuando propiedades como la maleabilidad, el brillo y la capacidad de formar aleaciones eran las principales características de clasificación. El desarrollo de la tabla periódica perfeccionó el sistema: los grupos de la izquierda y el centro son predominantemente metálicos, los grupos de la derecha son mayoritariamente no metálicos, con una estrecha banda diagonal de elementos que presentan características mixtas: los metaloides. En la práctica, la clasificación se basa en la utilidad metalúrgica, la facilidad de extracción, la importancia económica y la predicción del comportamiento químico. En la práctica moderna, la clasificación sirve de apoyo para la selección de materiales, el diseño de procesos y la elaboración de modelos predictivos.
Definición de las propiedades: criterios físicos
Una lista de comprobación técnica útil durante la identificación:
-
Conductividad eléctrica: Alto en la mayoría de los metales debido a un mar de electrones deslocalizados. Baja en la mayoría de los no metales. Los metaloides suelen presentar una conductividad semiconductora que varía mucho con la temperatura y el dopaje.
-
Conductividad térmica: Los metales suelen conducir el calor con eficacia; los no metales tienen una conducción térmica más deficiente; los metaloides varían.
-
Brillo y reflectividad: Los metales presentan un brillo metálico característico y una gran reflectividad en las superficies pulidas; muchos no metales son opacos o transparentes; los metaloides suelen mostrar un brillo metálico tenue.
-
Maleabilidad y ductilidad: Los metales se deforman plásticamente bajo tensión permitiendo el laminado, forjado o estirado; los no metales son quebradizos en forma sólida a granel; los metaloides pueden ser quebradizos pero a veces pueden trabajarse en condiciones especializadas.
-
Resistencia mecánica: Los metales abarcan una amplia gama que va desde los blandos (por ejemplo, el sodio) hasta los extremadamente resistentes (por ejemplo, los aceros de alta resistencia); el rendimiento mecánico depende en gran medida de la microestructura y la aleación.
-
Densidad: Los metales suelen tener densidades más altas que los no metales, aunque existen excepciones (por ejemplo, el yodo no metal denso).
-
Fase a STP (temperatura y presión estándar): La mayoría de los metales son sólidos a STP (el mercurio es una importante excepción líquida). Los no metales pueden ser gases (O₂, N₂), líquidos (bromo) o sólidos (carbono, azufre).
Propiedades definitorias: comportamiento químico y tendencias de enlace
Las diferencias químicas surgen de la electronegatividad, la energía de ionización y la afinidad electrónica:
-
Tendencia a perder electrones: Los metales tienen energías de ionización relativamente bajas y forman cationes con facilidad. Forman enlaces iónicos con muchos no metales y enlaces metálicos en estado puro o en aleaciones.
-
Tendencia a ganar o compartir electrones: Los no metales tienen electronegatividades y energías de ionización más altas, lo que favorece la ganancia o compartición de electrones; forman redes covalentes, moléculas diatómicas o aniones poliatómicos.
-
Carácter de óxido: Los óxidos metálicos tienden a ser básicos o anfóteros, mientras que los óxidos no metálicos suelen ser ácidos; los metaloides pueden formar óxidos anfóteros que muestran ambos comportamientos en función del socio reactivo.
-
Comportamiento redox en entornos típicos: Los metales actúan como agentes reductores en contacto con medios ácidos; los no metales suelen oxidar a los metales o actuar como oxidantes en su caso.
-
Formación de complejos: Los metales de transición forman complejos de coordinación fácilmente debido a la participación del orbital d; los no metales y los metaloides participan de forma diferente en la química de los complejos.
Estructura electrónica y colocación periódica
Comprender dónde aparece cada categoría en la tabla periódica aclara tanto las tendencias como las excepciones:
-
Metales: Ocupan el bloque s, el bloque d, el bloque f y parte del bloque p. Se caracterizan por bandas de conducción parcialmente llenas y funciones de trabajo bajas. Los metales de transición (bloque d) presentan estados de oxidación variables y propiedades magnéticas y catalíticas complejas.
-
No metales: Se agrupan en la parte superior derecha de la tabla periódica (excluidos los gases nobles, que constituyen una categoría aparte). Radios atómicos pequeños, electronegatividades altas y valvas de valencia llenas o casi llenas producen fuertes enlaces direccionales.
-
Metaloides: A caballo entre los metales y los no metales: boro, silicio, germanio, arsénico, antimonio, telurio, polonio (las clasificaciones varían). Sus estructuras de banda crean estrechos huecos de banda adecuados para aplicaciones semiconductoras.
Metaloides: definición, identificación y comportamiento límite
Los metaloides merecen especial atención porque sus propiedades intermedias sustentan la electrónica moderna y las aleaciones especiales:
-
Metaloides canónicos: Boro (B), Silicio (Si), Germanio (Ge), Arsénico (As), Antimonio (Sb), Telurio (Te). A veces se incluye el polonio, pero tiene consideraciones radiactivas.
-
Por qué importan los metaloides: Su comportamiento semiconductor puede ajustarse mediante dopaje y temperatura; forman fases vítreas y cerámicas con no metales; funcionan como elementos de aleación que modifican las propiedades mecánicas y térmicas.
-
Formas estructurales: Muchos metaloides forman redes covalentes (por ejemplo, el silicio) que son frágiles pero eléctricamente activas cuando se dopan. Otros (por ejemplo, el antimonio) tienen estructuras cristalinas en capas que muestran un comportamiento anisótropo.
-
Función industrial: Semiconductores (Si, Ge), retardantes de llama y modificadores de aleaciones (Sb), materiales termoeléctricos (Te) y cerámicas especiales (B).
Cuadros comparativos - referencia rápida
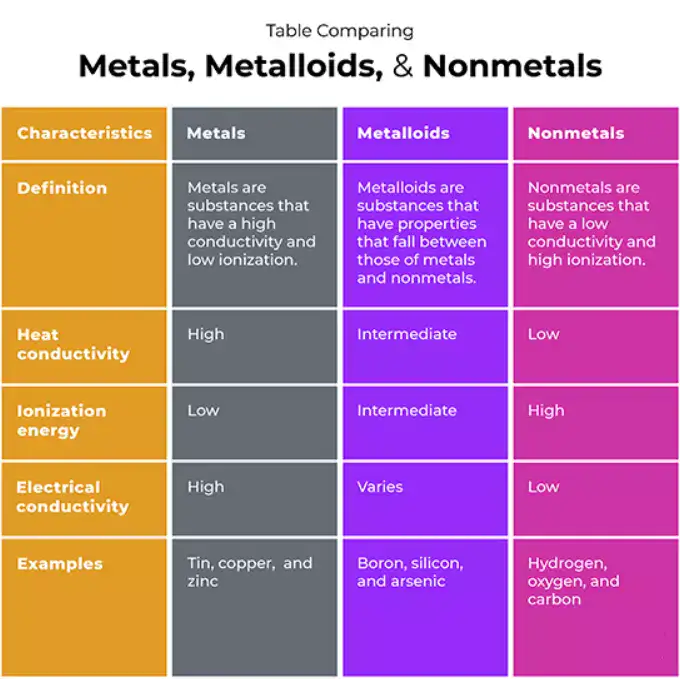
Cuadro 1 - Comparación física y química de alto nivel
| Propiedad / Característica | Metales | No metales | Metaloides |
|---|---|---|---|
| Conductividad eléctrica típica | Alta | Bajo a ninguno | Intermedio / semiconductor |
| Conductividad térmica | Alta | Bajo | Moderado |
| Lustre | Metálico (brillante) | Mate / no metálico | Brillo a menudo metálico |
| Comportamiento mecánico | Dúctil / maleable (muchos) | Quebradizo (la mayoría de los sólidos) | De frágil a semidúctil |
| Óxidos comunes | Básico / anfótero | Ácido / covalente | Anfótero |
| Adhesión típica | Metálico / iónico | Covalente / molecular | Covalente con carácter metálico parcial |
| Localización periódica | Izquierda / centro / abajo | Derecha / arriba | Límite de la escalera |
Cuadro 2 - Ejemplos representativos y usos típicos
| Categoría | Elementos representativos | Usos industriales típicos |
|---|---|---|
| Metales | Hierro (Fe), Cobre (Cu), Aluminio (Al), Níquel (Ni), Titanio (Ti) | Acero estructural, cableado eléctrico, aeroespacial, aleaciones resistentes a la corrosión |
| No metales | Oxígeno (O), Nitrógeno (N), Azufre (S), Carbono (C), Fósforo (P) | Materias primas químicas, polímeros, oxidantes, catalizadores (soportes de carbono) |
| Metaloides | Silicio (Si), Germanio (Ge), Boro (B), Antimonio (Sb), Telurio (Te) | Semiconductores, termoeléctricos, cerámicas especiales, aditivos para aleaciones |
Cuadro 3 - Firma electrónica / adhesiva y notas de extracción
| Clase de elemento | Comportamiento de los electrones de valencia | Fuente típica de mineral | Ruta típica de extracción o transformación |
|---|---|---|---|
| Metales | Electrones de conducción deslocalizados | Minerales: óxidos, sulfuros | Pirometalurgia, hidrometalurgia, refinado electrolítico |
| No metales | Localización de electrones, redes covalentes | Gases nativos, depósitos minerales (por ejemplo, azufre), fuentes orgánicas | Síntesis química, separación de gases, minería (por ejemplo, grafito) |
| Metaloides | Brecha de banda estrecha, enlaces covalentes direccionales | Silicatos, sulfuros, formas nativas | Purificación química (refinado zonal para el Si), torrefacción y lixiviación |

Aparición geológica, extracción y formas comerciales
Desde el punto de vista de la adquisición y la tramitación:
-
Metales: A menudo se extrae de óxidos y sulfuros (por ejemplo, hematita para el hierro, calcopirita para el cobre). La fundición elimina el oxígeno o el azufre; la electrorrefinería y la magnetohidrometalurgia producen un metal de gran pureza. Formas comerciales: lingotes, palanquillas, chapas, bobinas, alambre, polvo.
-
No metales: Se presentan en forma elemental, molecular o mineral. El carbono aparece en forma de grafito o diamante; el azufre se presenta en depósitos elementales o emisiones volcánicas; el nitrógeno y el oxígeno son gases atmosféricos obtenidos por separación del aire. Las formas comerciales incluyen gases, polvos y sólidos moleculares.
-
Metaloides: El silicio se extrae del cuarzo y se refina hasta obtener silicio de calidad metalúrgica mediante reducción carbotérmica, y después se purifica con métodos químicos (por ejemplo, el proceso Siemens o los reactores de lecho fluidizado) para obtener Si de calidad electrónica. El boro se obtiene de los boratos; el germanio suele recuperarse de los minerales de zinc o de las cenizas volantes de carbón.
Usos industriales y ejemplos con notas prácticas de adquisición
Resúmenes por elementos con consideraciones de compra:
-
Hierro / Acero (metal): Metal estructural primario. Las especificaciones de compra suelen hacer referencia a normas (ASTM A36, A992, etc.), y la microestructura importa (por ejemplo, ferrítica, martensítica). La resistencia a la corrosión y la soldabilidad dependen de la composición y el tratamiento térmico.
-
Cobre (metal): Crítico para la conducción eléctrica. Los grados de compra (por ejemplo, C11000, C10200) indican pureza y conductividad. El cobre sin oxígeno se utiliza cuando se requiere alta conductividad y bajos niveles de impurezas.
-
Aluminio (metal): Preferido cuando la baja densidad y la resistencia a la corrosión son vitales. Las series de aleaciones (1000 a 7000) definen las propiedades clave. El acabado superficial y el revenido son importantes para las aplicaciones de conformado frente a las estructurales.
-
Silicio (metaloide): El silicio de grado electrónico se utiliza para obleas; el silicio de grado metalúrgico se utiliza para aleaciones y siliconas. Para comprarlo hay que prestar mucha atención a la pureza (niveles de ppb para la electrónica).
-
Carbono (no metálico): El grafito se utiliza como electrodo de alta temperatura y lubricante; el carbón activado para la adsorción. La forma y la porosidad determinan el rendimiento.
Consejo sobre aprovisionamiento: Solicite certificados de materiales (informes de pruebas de laminación, informes de pruebas químicas y mecánicas), confirme los límites de impurezas en trazas para aplicaciones críticas y verifique el cumplimiento de las normas aplicables (ASTM, ISO, EN).
Aleación, tratamiento y modificación de propiedades
Cómo se corresponden las diferencias con los procesos industriales de uso común:
-
Metales de aleación: La incorporación de elementos modifica la densidad electrónica, la distorsión de la red y la estabilidad de las fases. Por ejemplo, el carbono en el hierro forma acero con una resistencia mucho mayor; el cromo añade resistencia a la corrosión en los aceros inoxidables.
-
Dopaje de metaloides: La introducción controlada de impurezas donantes o aceptoras convierte los semiconductores intrínsecos en tipo n o tipo p, lo que dicta el comportamiento eléctrico. La temperatura y la concentración regulan la movilidad de los portadores.
-
Funcionalización no metálica: Los no metales forman compuestos funcionales (por ejemplo, el carbono en los polímeros, el azufre en el caucho vulcanizado) que ofrecen un rendimiento químico o mecánico específico.
-
Tratamiento térmico: Los metales responden bien al recocido, el temple, el revenido y el endurecimiento por envejecimiento. Los metaloides y los materiales no metálicos requieren rutas térmicas o químicas especializadas para ajustar sus propiedades (por ejemplo, sinterización de cerámica, recocido de vidrio).
Seguridad, manipulación y consideraciones medioambientales
Puntos prácticos de seguridad para cada clase:
-
Metales: Muchos metales producen polvo o humos tóxicos durante el corte, la soldadura o la fundición (por ejemplo, plomo, cadmio). Los metales corroídos pueden producir subproductos peligrosos. Utilice EPI y ventilación adecuados y cumpla las normas de eliminación de residuos.
-
No metales: Los no metales reactivos (p. ej., fósforo, cloro gaseoso) plantean riesgos agudos; los polvos (p. ej., negro de humo) pueden presentar riesgos de explosión de polvo. Siga las instrucciones de la MSDS.
-
Metaloides: Algunos metaloides presentan problemas de toxicidad (por ejemplo, los compuestos de arsénico). Los materiales semiconductores pueden requerir un control de la contaminación y una manipulación en sala blanca.
-
Medioambiental: Los impactos del ciclo de vida difieren drásticamente; los metales a menudo implican una extracción intensiva en energía, mientras que la producción de algunos no metales (como los polímeros derivados de la petroquímica) conlleva diferentes perfiles contaminantes. Las consideraciones sobre reciclaje y sustitución desempeñan un papel importante en la estrategia de adquisición.
Cómo identificar una muestra desconocida en el laboratorio o en el taller
Un protocolo práctico por etapas:
-
Inspección visual: Observe el color, el brillo y la textura. El brillo metálico sugiere metal o metaloide.
-
Medición de la densidad: La densidad aparente medida por desplazamiento es un buen indicio. Una densidad alta sugiere la presencia de metales (pero hay que comprobar si hay no metales pesados, como el yodo).
-
Prueba eléctrica: Utilice un multímetro para medir la conductividad CC. Una conductividad alta indica metal; una baja sugiere no metal; un comportamiento intermedio dependiente de la temperatura sugiere metaloide/semiconductor.
-
Prueba mecánica: Las pruebas sencillas de doblado o rayado indican ductilidad frente a fragilidad. Los metales suelen deformarse; los no metales suelen fracturarse.
-
Pruebas químicas puntuales: La reacción de pequeñas muestras con ácidos o el uso de pruebas de llama pueden identificar el comportamiento de la clase: los metales pueden disolverse y formar iones coloreados; los no metales producen gases o residuos insolubles. Siga siempre los protocolos de seguridad.
-
Confirmación espectroscópica: XRF, AES, ICP-MS o XRD proporcionan la composición definitiva y la identificación de fases para la verificación del grado de adquisición.
Preguntas frecuentes
P1: ¿Qué diferencia electrónica fundamental separa a los metales de los no metales?
A: Los metales poseen electrones de valencia deslocalizados que forman bandas de conducción y permiten el movimiento libre de electrones bajo un campo eléctrico. Los no metales tienen electrones localizados que ocupan capas de valencia llenas o casi llenas, lo que favorece los enlaces covalentes direccionales y da lugar a una mala conducción eléctrica en masa.
P2: ¿Los metaloides son siempre semiconductores?
A: No siempre. Muchos metaloides tienen un comportamiento semiconductor intrínseco con bandas estrechas (ejemplo: silicio, germanio), pero la forma física, el dopaje y la temperatura influyen mucho en la conductividad; algunos metaloides tienen un comportamiento más metálico en determinadas morfologías cristalinas.
P3: ¿Cómo reflejan las propiedades de los óxidos la clasificación de los elementos?
A: Los óxidos metálicos suelen ser básicos o anfóteros y neutralizan los ácidos para formar sales. Los óxidos no metálicos suelen ser ácidos, formando ácidos en el agua (por ejemplo, SO₂ → ácido sulfuroso). Los metaloides suelen formar óxidos anfóteros con reacciones tanto básicas como ácidas.
P4: ¿Qué pruebas determinan rápidamente si un metal es un metal de transición o un metal del grupo principal?
A: Los metales de transición suelen presentar múltiples estados de oxidación estables, iones coloreados en solución y comportamiento de formación de complejos; los metales del grupo principal suelen presentar menos estados de oxidación y compuestos binarios más sencillos.
P5: ¿Qué importancia tiene la pureza del silicio industrial utilizado en electrónica?
A: Extremadamente importante. El silicio de calidad electrónica requiere niveles de impurezas en el rango de partes por billón (ppb) o inferiores; las trazas de metales pueden alterar drásticamente la vida útil del portador y el rendimiento del dispositivo.
P6: ¿Pueden los no metales formar aleaciones?
A: No en el sentido metálico clásico. Sin embargo, los elementos no metálicos se combinan para formar mezclas y compuestos (por ejemplo, carbono en compuestos reforzados con grafito o mezclas de polímeros) que desempeñan funciones similares a las de las aleaciones en determinadas aplicaciones.
P7: ¿Qué clase se corroe más fácilmente y cómo se consigue la protección?
A: La propensión a la corrosión depende del entorno y del elemento: el hierro se oxida fácilmente en oxígeno húmedo; muchos no metales no se corroen pero pueden oxidarse o descomponerse. Los métodos de protección incluyen revestimientos, protección catódica, aleación y control ambiental.
P8: ¿Hay elementos que desafían una clasificación simple?
A: Sí, varios elementos se encuentran cerca del límite de los metaloides y muestran polimorfismo con fases metálicas y no metálicas. Además, los elementos sometidos a presiones o temperaturas extremas pueden cambiar de comportamiento.
P9: ¿Cómo influyen las adiciones de aleación de metaloides en las propiedades de los metales?
A: Pequeñas adiciones de metaloides (por ejemplo, silicio, boro) refinan el tamaño del grano, alteran la templabilidad, mejoran la resistencia a la temperatura o modifican el comportamiento eléctrico. Por ejemplo, el silicio en el acero influye en la desoxidación y las propiedades magnéticas.
Q10: ¿Qué normas de materiales deben consultarse a la hora de especificar metales para la adquisición?
A: Las normas más comunes son ASTM (estadounidense), EN (europea), ISO, JIS (japonesa), según la región. En el caso de los materiales electrónicos, se aplican las normas JEDEC y las específicas de los semiconductores. Solicite siempre los correspondientes informes de ensayos de laminación y documentos de conformidad.
Referencias autorizadas
- IUPAC - Tabla periódica e información sobre los elementos
- NIST Chemistry WebBook - Datos termoquímicos y espectroscópicos
- Royal Society of Chemistry - Tabla periódica interactiva y datos de los elementos
- USGS - Información sobre metales y minerales (Centro Nacional de Información sobre Minerales)
Notas finales y próximos pasos recomendados
-
Para la documentación de adquisición, empareje este material conceptual con las normas ASTM/EN aplicables para cada metal o aleación específicos.
-
Para quienes preparan material didáctico o contenidos web, transforme las tablas en HTML responsivo con microdatos para obtener mejores resultados en los motores de búsqueda.
-
Si necesita más información sobre un elemento concreto, un sistema de aleación o una ruta de procesamiento (por ejemplo, programas de tratamiento térmico para aceros específicos, rutas de pureza de las obleas de silicio o datos de ensayos de corrosión), indique el nombre del elemento o la aleación y la aplicación prevista; a continuación, se puede preparar un informe técnico específico.

